题目内容
16. 如图是某物质的分子模型,下列关于该物质说法正确的是( )
如图是某物质的分子模型,下列关于该物质说法正确的是( )| A. | 属于有机物 | B. | 化学式为NH3 | ||
| C. | 氮元素和氢元素的质量比为1:3 | D. | 其中氮元素的化合价为+3 |
分析 A.根据有机物的概念来分析;
B.根据分子结构模型来分析;
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
D.根据化合物中元素化合价的计算方法来分析.
解答 解:由某物质的分子模型,一个分子是由1个氮原子和3个氢原子构成的,其化学式为:NH3.
A.由化学式可知,氨气中不含碳元素,所以不属于有机物,故错误;
B.由某物质的分子模型,一个分子是由1个氮原子和3个氢原子构成的,其化学式为:NH3,故正确;
C.氨气中,氮元素和氢元素的质量比为14:(1×3)≠1:3,故错误;
D.氨气中,氢元素显+1价,设氮元素的化合价为x,x+(+1)×3=0,x=-3,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是在食盐(NaCl)中按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
①测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
②探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水
①测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
②探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水
| 实验操作 | 预期现象级结论 |
| 步骤1:取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品溶解,形成无色溶液. |
| 步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡. | 有白色沉淀生成,说明样品b中添加了镁盐. |
| 步骤3:取少量步骤1形成的溶液于试管中,再滴加少量的BaCl2溶液振荡 | 若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2 |
7.下列物质的成分属于有机合成材料的是( )
| A. |  饮料瓶 | B. |  羊毛 | ||
| C. |  金属材料 | D. |  木材 |
4.下列实验操作、现象与结论均正确的是 ( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向收集满CO2的软塑料瓶中加入约$\frac{1}{3}$体积的水,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与H2O反应 |
| B | 常温下,分别向等体积的盛有空气样品和呼出气体样品的集气瓶中滴加等量的饱和澄清石灰水,震荡 | 呼出气体样品中的石灰水比空气样品中的石灰水更浑浊 | 呼出气体样品中CO2含量比空气样品高 |
| C | 在带尖嘴的导管口点燃某气体,然后在火焰上方罩一个冷而干燥的小烧杯 | 烧杯内壁有水雾 | 该气体是H2 |
| D | 往某化肥的样品中加少量熟石灰研碎 | 闻到刺激性气味 | 该化肥为磷肥 |
| A. | A | B. | B | C. | C | D. | D |
1.等质量的下列固体物质分别与一定量的稀盐酸(溶质质量分数相同)恰好完全反应,下列说法正确的是( )
| A. | 金属铝和镁比较,镁反应速度快,但生成氢气的质量少 | |
| B. | 镁与氧化镁比较,镁消耗的盐酸质量少,反应后溶液中溶质的质量分数小 | |
| C. | 碳酸钙粉末与石灰石比较,碳酸钙粉末反应速度快,消耗的盐酸质量少 | |
| D. | 氧化铜与氢氧化铜比较,反应后溶液中的溶质质量相等,溶液质量也相等 |
8.有关分子、原子、离子的说法正确的是( )
| A. | 分子可以再分,原子不可再分 | |
| B. | 分子、原子能直接构成物质,而离子不能 | |
| C. | 原子得失电子可形成离子,而离子不能形成原子 | |
| D. | 分子、原子、离子质量都很小 |
5.下列关于水的说法正确的是( )
| A. | 水是由氢原子和氧原子直接构成的 | B. | 长期饮用蒸馏水有利于人体健康 | ||
| C. | 水能够溶解所有的物质 | D. | 可以用肥皂水区分软水和硬水 |
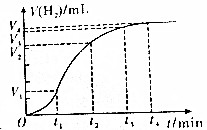 进行锌与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳锌与稀盐酸反应速率的变化规律锌与稀盐酸反应的速率先慢后快最后又慢,结合上述探究解释曲线变化的原因开始时反应物浓度最大,随着反应的进行浓度降低,但反应放热,温度逐渐升高,所以反应速率逐渐增大,随着反应的进行,浓度逐渐减小,浓度因素大于温度因素,反应速率逐渐减小.
进行锌与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳锌与稀盐酸反应速率的变化规律锌与稀盐酸反应的速率先慢后快最后又慢,结合上述探究解释曲线变化的原因开始时反应物浓度最大,随着反应的进行浓度降低,但反应放热,温度逐渐升高,所以反应速率逐渐增大,随着反应的进行,浓度逐渐减小,浓度因素大于温度因素,反应速率逐渐减小.