题目内容
某K2CO3样品,一定含Na2CO3、KNO3和Ba(NO3)2杂质中的一种或两种,将13.8g样品加入足量水,样品全部溶解,再加入过量的CaCl2溶液,得到9.5g沉淀,对样品所含杂质的正确判断是( )
|
| A. | 一定有KNO3,还可能有Ba(NO3)2 | B. | 一定没有Ba(NO3)2,可能有KNO3 |
|
| C. | 一定有KNO3,还可能有Na2CO3 | D. | 一定没有Na2CO3和Ba(NO3)2 |
| 取样品加入水中,全部溶解,则不可能硝酸钡,加入氯化钙能产生沉淀,然后根据沉淀的质量进一步确定碳酸钠和硝酸钾的存在. | |
| 解答: | 解:样品加入水中,全部溶解,说明一定无硝酸钡,假设13.8g纯碳酸钾产生碳酸钙的质量为x,则有 K2C03+CaCl2═CaCO3↓+2KCl 138 100 13.8g x
x=10g 假设13.8g纯碳酸钠产生碳酸钙的质量为y,则有 Na2C03+CaCl2═CaCO3↓+2NaCl 106 100 13.8g y
y=13g 根据上述解答可知道:含有一种杂质的情况是:只能是含有硝酸钾,而不能含有碳酸钠.若含有碳酸钠则得到沉淀的质量应该大于10g小于13g,而实际只得到9.5g,故不可能含有碳酸钠,所以一定含有硝酸钾. 含有两种杂质是:是硝酸钾和碳酸钠的混合物. 故可以知道在该硝酸钾样品中一定含有硝酸钾,分析所给的选项可以知道选项C是正确的. 故选C. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
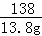 =
=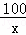
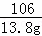 =
=