题目内容
15.有一部分变质的KOH样品,含H2O:7.62%; K2CO3:2.38%;K2O:10%;KOH:80%;取该样品W克加入98克质量分数为20%的稀硫酸充分反应后,再加入20克质量分数为10%的KOH溶液恰好呈中性,把反应后所得溶液小心蒸干得到固体(不含结晶水)多少克?分析 通过题意可知最后所得固体质量是硫酸钾的质量,可以根据硫酸钾和硫酸的关系来求出硫酸钾的质量.
解答 解:设得到硫酸钾质量为X则:
根据H2SO4----K2SO4
98 174
98g×20% X
根据:$\frac{98}{174}=\frac{98g×20%}{x}$
解得X=34.8g
答:把反应后所得溶液小心蒸干后可得固体质量为34.8g.
点评 解答本题的关键是要知道最后得到的固体是硫酸钾,所以只要根据硫酸的质量可直接求得硫酸钾的质量.

练习册系列答案
相关题目
20.下列关于碳及碳的氧化物的说法中不正确的是( )
| A. | 在有煤炭炉的室内放置一盆水防止一氧化碳中毒 | |
| B. | 木炭具有吸附性是因为它具有疏松多孔的结构 | |
| C. | 金刚石和石墨的物理性质不同,是由于它们的碳原子排列方式不同 | |
| D. | 碳纳米管是一种新型的碳单质 |
3.空气中最多的物质是( )
| A. | N2 | B. | O2 | C. | H2O | D. | 稀有气体 |
10.对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
| 实验内容 | 实验现象 | 分析与结论 |
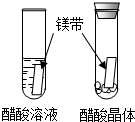 | 醋酸晶体试管内无现象或无明显现象,醋酸溶液试管中镁带表面冒气泡. | 酸的很多反应通常在水溶液中才能完成. |
用玻璃棒蘸硫酸在白纸上写字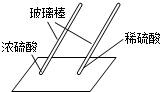 | 浓(填“浓”或“稀”)硫酸使白纸炭化. | 即使是同种酸,由于浓度或溶质质量分数不同,它们的性质不完全相同. |
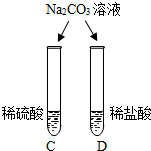 | 两试管中均产生气泡 | 不同的酸具有相似的性质,这是因为酸的组成中都含有H(填元素符号). |
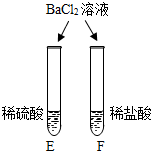 | E试管中产生白色沉淀, F试管中无明显现象. | 不同的酸根会导致酸的“个性”差异.因此,可用氯化钡溶液鉴别盐酸和硫酸. |
4.下列物质中含有氧气的是( )
| A. | 过氧化氢 | B. | 高锰酸钾 | C. | 二氧化锰 | D. | 液态空气 |
 质量分数为20%的稀硫酸中漂浮着一木块.
质量分数为20%的稀硫酸中漂浮着一木块.