题目内容
将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X.测得反应前后物质的质量如下表:
(1)生成的二氧化碳和X的质量比是 .
(2)若X是一氧化碳,写出该反应的化学方程式 .
| 物质 | C6H6 | O2 | CO2 | H2O | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
(2)若X是一氧化碳,写出该反应的化学方程式
考点:质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:根据质量守恒定律可知:反应后质量减少的物质是反应物,质量增加的物质是生成物;根据质量守恒定律可以确定X的质量;通过计算苯、氧气、二氧化碳、水中各元素的质量,推算出X中所含元素的种类.
解答:解:
由表格信息可知:反应后CO2质量增加了6.6g,是生成物;H2O质量增加了2.7g,是生成物;
O2质量减少了9.6g,是反应物;苯的质量减少了3.9g克,是反应物;生成物还少4.2g,所以X是生成物.则:
(1)生成的二氧化碳和X的质量比=(6.6g-0g):(4.2g-0g)=11:7.
(2)若X是一氧化碳,则反应物为:氧气、苯,生成物为二氧化碳、水、一氧化碳;则该反应的化学方程式为:C6H6+6O2
3CO2+3CO+3H2O
故答案为:
(1)11:7.(2)C6H6+6O2
3CO2+3CO+3H2O
由表格信息可知:反应后CO2质量增加了6.6g,是生成物;H2O质量增加了2.7g,是生成物;
O2质量减少了9.6g,是反应物;苯的质量减少了3.9g克,是反应物;生成物还少4.2g,所以X是生成物.则:
(1)生成的二氧化碳和X的质量比=(6.6g-0g):(4.2g-0g)=11:7.
(2)若X是一氧化碳,则反应物为:氧气、苯,生成物为二氧化碳、水、一氧化碳;则该反应的化学方程式为:C6H6+6O2
| ||
故答案为:
(1)11:7.(2)C6H6+6O2
| ||
点评:本题难度不是很大,解答本题要认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验的操作如图所示,其中正确的是( )
A、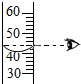 读取液体体积 |
B、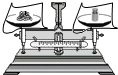 称量固体烧碱 |
C、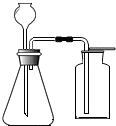 Zn和稀H2SO4制H2 |
D、 稀释浓硫酸 |
如图为元素周期表第三周期的一部分.下列说法中正确的是( )
| 11 Na 钠 22.99 |
12___ 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
| A、硅元素的核电荷数为14 |
| B、Al的相对原子质量是26.98g |
| C、它们都属于金属元素 |
| D、镁的元素符号为mg |

 )与 B(
)与 B(  )反应生成C(
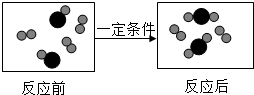
)反应生成C( ),下图是其反应前后分子及其数目变化的微观示意图(
),下图是其反应前后分子及其数目变化的微观示意图( 表示两种质子数不同的原子 ).
表示两种质子数不同的原子 ).