题目内容
某反应为C2H8N2+2R=3N2+4H2O+2CO2;其中R的化学式是( )
| A、N2O4 |
| B、NO2 |
| C、N2O |
| D、CH4 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律可知化学反应前后原子的种类和数目不变,则利用化学反应方程式为C2H8N2+2R=3N2+4H2O+2CO2,借助反应物和生成物中所含的原子的种类和数目相同来推断化学反应方程式中R的化学式.
解答:解:化学反应方程式为C2H8N2+2R=3N2+4H2O+2CO2,根据质量守恒定律可知,反应前后原子的种类和数目相同,C、H原子在反应前后相等,反应前有2个N原子,而反应后共有6个N原子,则R中有4个N原子,反应前没有O原子,而反应后共有8个O原子,则R中有8个O原子,又R的化学计量数为2,则R的化学式为N2O4,
故选A.
故选A.
点评:本题考查学生运用化学方程式和质量守恒定律来推断物质的化学式,学生应学会利用守恒法来分析解答.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
下列方法或做法中,不能用于鉴别CO2和CO的是( )
| A、将两种气体分别通入紫色石蕊试液中 |
| B、将两种气体分别能过灼热的氧化铜 |
| C、分别闻两种气体的气味 |
| D、将燃着的木条分别伸入盛有CO2和CO的集气瓶中 |
下列实验操作正确的是( )
A、 熄灭酒精灯 |
B、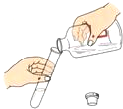 倾倒液体 |
C、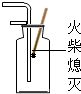 气体验满 |
D、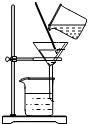 液体过滤 |
下列除去物质中所含杂质(括号内为杂质)的方法正确的是( )
| A、CO2(HCl)气体,先通过NaOH溶液,再通过浓硫酸 |
| B、O2(N2)气体,通过灼热的铜粉 |
| C、NaCl溶液(Na2CO3),加入稀盐酸,至不再产生气泡 |
| D、Fe(Cu)粉,加入足量的硫酸铜溶液 |
下列各组物质在溶液中 不能 反应的是( )
| A、HCl和AgNO3 |
| B、KNO3 和NaCl |
| C、H2SO4 和BaCl2 |
| D、NaOH 和H2SO4 |
归纳和总结是非常重要的学习方法,但要注意严谨、全面、科学.下列总结出的规律符合这一要求的是( )
| A、生成盐和水的反应一定是中和反应 |
| B、催化剂一定能加快化学反应速率 |
| C、浓溶液一定是饱和溶液 |
| D、氧化物中一定含有氧元素,但含有氧元素的化合物不一定是氧化物 |
下列常见的物质属于纯净物的是( )
| A、矿泉水 | B、蒸馏水 |
| C、湘江水 | D、黄河水 |
某学生用托盘天平称取3.3g食盐,称量时指针若左偏,此时应该( )
| A、增加药品 | B、减少药品 |
| C、增加砝码 | D、减少砝码 |
