题目内容
2.请按要求写出化学方程式.(1)活泼金属与酸反应生成理想的清洁燃料.Zn+H2SO4═ZnSO4+H2↑(合理即可)
(2)已知氯气(Cl2)能与水反应生成HCl和HClO(次氯酸).则氯气和氢氧化钠溶液反应的化学方程式Cl2+2NaOH═NaCl+NaClO+H2O.
(3)浓硫酸有吸水性,请写出蔗糖与浓硫酸反应化学方程式C12H22O11$\frac{\underline{\;浓硫酸\;}}{\;}$12C+11H2O(提示:浓硫酸可以将元素中的氢氧按2:1排列,从而达到吸水性)
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)锌能与稀硫酸反应生成硫酸锌和氢气,氢气是理想的清洁燃料,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑(合理即可).
(2)氯气(Cl2)能与水反应生成HCl和HClO(次氯酸),氯气和氢氧化钠溶液生成氯化钠、次氯酸钠、水,反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O.
(3)蔗糖与浓硫酸反应,浓硫酸可以将元素中的氢氧按2:1排列,从而达到吸水性,在这里浓硫酸充当催化剂,蔗糖与浓硫酸反应化学方程式为:C12H22O11$\frac{\underline{\;浓硫酸\;}}{\;}$12C+11H2O.
故答案为:(1)Zn+H2SO4═ZnSO4+H2↑(合理即可);(2)Cl2+2NaOH═NaCl+NaClO+H2O;(3)C12H22O11$\frac{\underline{\;浓硫酸\;}}{\;}$12C+11H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
8.要除去氯化钠溶液中混有的少量碳酸钠杂质,可以加入适量的( )
| A. | 澄清石灰水 | B. | 氯化钾溶液 | C. | 硝酸银溶液 | D. | 盐酸 |
7.下列实验操作或实验结束后仪器放置正确的是( )
| A. | 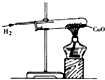 氢气还原氧化铜 氢气还原氧化铜 | B. | 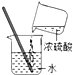 稀释浓硫酸 稀释浓硫酸 | ||
| C. | 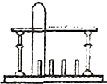 洗干净的试管放在试管架上 洗干净的试管放在试管架上 | D. |  用过滴管放在桌面上 用过滴管放在桌面上 |
14.某化学兴趣小组学习氢氧化钠的性质之后展开探究性学习,请你作为该小组成员一起来解决下列问题;
(1)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)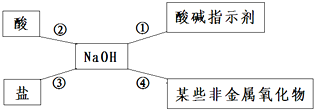
I.依据反应④说明,NaOH必须密封保存,否则在空气中要变质;其化学反应方程式为CO2+2NaOH=Na2CO3+H2O
II.为了验证反应③能够发生,你选择的物质是c(填序号).
a.Na2CO3 b. HCl c.CuSO4 d. Ba(NO3)2
(2)氢氧化钠溶液能使无色酚酞溶液变红色,且其中含有H2O、Na+、OH-三种微粒,小组同学想进一步探究是哪种微粒使无色酚酞溶液变红色.
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-.
【实验验证】
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是无色酚酞试液中有大量水分子,已经证明水分子不能使酚酞变红色.
(1)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)

I.依据反应④说明,NaOH必须密封保存,否则在空气中要变质;其化学反应方程式为CO2+2NaOH=Na2CO3+H2O
II.为了验证反应③能够发生,你选择的物质是c(填序号).
a.Na2CO3 b. HCl c.CuSO4 d. Ba(NO3)2
(2)氢氧化钠溶液能使无色酚酞溶液变红色,且其中含有H2O、Na+、OH-三种微粒,小组同学想进一步探究是哪种微粒使无色酚酞溶液变红色.
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-.
【实验验证】
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量氯化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 振荡试管内溶液仍为无色 | Na+不能使无色酚酞试液变红色 |
| ③用试管取少量氢氧化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液变为红色 |
11. 某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
(1)分别向两支装有碳酸钠和碳酸钙粉末的试管中注入一定量的稀盐酸,两支试管内均观察到的现象是有气泡产生,固体粉末全部消失,最终形成无色溶液.实验结束后,同学们将A、B两支试管中的废液倒入同一只洁净的烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)小组同学将烧杯中的物质进行了过滤,对滤液中的溶质成分展开了探究,请你一起参与.
【提出猜想】猜想1:滤液中的溶质是氯化钠;
猜想2:滤液中的溶质是氯化钠和碳酸钠;
猜想3:滤液中的溶质是氯化钠和氯化钙.
【设计实验】请你对猜想2进行验证.
 某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
某学习小组在探究酸的化学性质时,做了如图所示的两个实验:(1)分别向两支装有碳酸钠和碳酸钙粉末的试管中注入一定量的稀盐酸,两支试管内均观察到的现象是有气泡产生,固体粉末全部消失,最终形成无色溶液.实验结束后,同学们将A、B两支试管中的废液倒入同一只洁净的烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)小组同学将烧杯中的物质进行了过滤,对滤液中的溶质成分展开了探究,请你一起参与.
【提出猜想】猜想1:滤液中的溶质是氯化钠;
猜想2:滤液中的溶质是氯化钠和碳酸钠;
猜想3:滤液中的溶质是氯化钠和氯化钙.
【设计实验】请你对猜想2进行验证.
| 实验步骤 | 预计实验现象 | 预计结论 |
| 取少量溶液于试管中, 加入少量的稀盐酸 | 产生气泡 | 猜想2正确 |