题目内容
10.下列实验操作正确的是( )| A. |  点燃酒精灯 | B. |  滴加水 | C. |  加热液体 | D. |  读取液体体积 |
分析 A、使用酒精灯时要注意“两查、两禁、一不可”.
B、根据使用胶头滴管滴加少量液体的方法进行分析判断.
C、根据给试管中的液体加热的方法进行分析判断.
D、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断
解答 解:A、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误.
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误.
C、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,图中液体超过试管容积的$\frac{1}{3}$,图中所示操作错误.
D、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中所示操作正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
5.把过量的铁粉分别加入到下列各组物质的溶液中,充分反应后过滤,滤液中含有的物质相同的是( )
| A. | Na2SO4、CuSO4 | B. | H2SO4、CuSO4 | C. | HCl、H2SO4 | D. | CuCl2、Cu(NO3)2 |
15.去年春季以来,甲型H1N1流感疫情在一些国家持续蔓延,用于治疗流感的抗病毒药物“达菲”可以有效地预防和治疗甲型H1N1流感.从烹调香料八角中提取到的莽草酸(化学式为:C7H10O5)是制取“达菲”的基本原料.下列有关莽草酸的说法正确的是( )
| A. | 莽草酸中分别有7个碳元素、10个氢元素、5个氧元素 | |
| B. | 该物质中含有22个原子 | |
| C. | 莽草酸的相对分子质量为174 | |
| D. | 莽草酸中C、H、O三种元素的质量比为7:10:5 |
19.下列各图所示是生活中的变化,其中属于物理变化的是( )
| A. |  燃放烟花爆竹 | B. |  焚烧秸杆发电 | C. |  葡萄酿酒 | D. |  炭雕净化空气 |
20.空气中氧气含量测定的再认识.
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
步骤如下:
①用弹簧夹夹紧橡皮管.
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子.
③待装置冷却后打开弹簧夹.
④观察并记录水面的变化情况.
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5.
【实验改进1】
Ⅰ.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图2实验装置,再次测定空气中氧气含量.装置中的食盐水和活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%.(消耗的水的体积忽略不计,计算结果保留一位小数).
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想(Ⅱ)(填序号)一定是错误的,理由是化学反应前后元素种类不变.
实验改进2】
使用图3装置进行实验.实验前应先进行的操作
是检查装置的气密性.
【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
数据处理】实验中需要记录的数据是注射器中原来的空气体积,反应后剩余气体的体积.
计算得出氧气约占空气总体积的$\frac{1}{5}$.
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等.(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
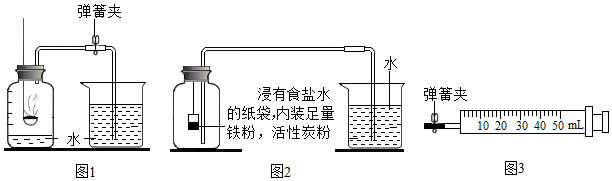
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
步骤如下:
①用弹簧夹夹紧橡皮管.
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子.
③待装置冷却后打开弹簧夹.
④观察并记录水面的变化情况.
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5.
【实验改进1】
Ⅰ.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图2实验装置,再次测定空气中氧气含量.装置中的食盐水和活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%.(消耗的水的体积忽略不计,计算结果保留一位小数).
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想(Ⅱ)(填序号)一定是错误的,理由是化学反应前后元素种类不变.
实验改进2】
使用图3装置进行实验.实验前应先进行的操作
是检查装置的气密性.
【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
数据处理】实验中需要记录的数据是注射器中原来的空气体积,反应后剩余气体的体积.
计算得出氧气约占空气总体积的$\frac{1}{5}$.
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等.(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
