题目内容
下列有关“2CO+O2点燃2CO2”的质量关系,不正确的是
A.若56gCO参加反应,则消耗O2的质量一定是32g
B.若16gO2参加反应,则生成CO2的质量一定是44g
C.若10gCO2生成,则消耗CO和O2的质量总和一定是10g
D.若5gCO和2g O2混合点燃,则CO2生成的质量一定是7g
【答案】D
【解析】
试题分析:A、根据化学方程式意义可知,若56gC0参加反应,则浪耗O2的质量一定是32。故说法 正确;B、每56份质量的一氧化碳和32份质量的氧气完全反应能生成88份质量的二氧化碳, 因此若16gO2参加反应,则生成 CO2的质量一定是44g,故说法正确;C、根据质量守恆定律可知,若10g CO2生成,则消耗CO和O2的质量总和一定是10g,故说法正确;D、每56份质量的 —氧化碳和32份质量的氧气完全反应能生成88份质量的二氧化碳,设和2g氧气反应的一氧 化碳的质量为X,则x: 2g=56: 32,解得x=3.5g,因此一氧化碳有剩余,生成二氧化碳的质量 是5.5g,故说法错误,故选D.
考点:考査化学方程式含义以及质量守恒定律及其应用

下列用途与其化学性质无关的是( )
| A.用食醋除热水瓶中的水垢 B.用擦酒精的办法给发烧病人降体温 C.用熟石灰改良酸性土壤 D.用小苏打发面蒸馒头 |
某兴趣小组为验证质量守恒定律,做 了镁条在空气中燃烧的实验。
了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式_______________。
(2)小 明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我_____(“同意”或“不同意”)小明的观点,因为___________
明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我_____(“同意”或“不同意”)小明的观点,因为___________ 。
。
(3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
 【提出问题】黄色固体是什么呢?
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论[来源:学§科§网] |
【反思与交流】空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却 远多于Mg3N2,为什么呢?请给出合理的解释_
远多于Mg3N2,为什么呢?请给出合理的解释_ ____________。
____________。
[注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。]
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下 :
:
| 实验序号 | 实验1 | 实验2 | 实验3 | |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4l | H2O |
| 实验现象 | 有大量气泡产生 |
| 有少量气泡产生 | 气泡极少 |
| 加热后,实验现象 | 气泡明显增多可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
上表中,用水进行实验的目的是_________________。
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):①__________;②_____________;③______________。
 A.属于非金属元素
A.属于非金属元素

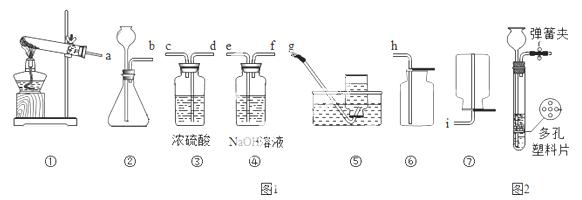
 氧气应选用 作为发生装置(填装置序号)。检验该装置气密性的方法是 。
氧气应选用 作为发生装置(填装置序号)。检验该装置气密性的方法是 。
