题目内容
11.农业上常用质量分数为16%的氯化钠(NaCl)溶液来选种.(1)为什么用16%的氯化钠溶液选种而不用水?该浓度的溶液可以使瘪种子浮起,成熟种子下沉,而水密度较它小,起不到选择作用
(2)实验室里要配制80g这种溶液需要氯化钠(NaCl)12.8g,水67.2g.
(3)实验室中有以下仪器:①药匙②集气瓶③烧杯④试管⑤玻璃棒⑥量筒⑦漏斗⑧铁架台⑨酒精灯⑩托盘天平,所必需的仪器有(填序号)①③⑤⑥⑩.
(4)若配制的氯化钠(NaCl)溶液经检测质量分数大于16%,试分析造成误差的可能原因.量筒量取水时,俯视液面(合理即可).
分析 (1)根据16%的氯化钠溶液与水的密度,进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(3)实验室配制100g5%的NaCl溶液操作步骤分别是:计算、称量、溶解,根据各操作确定所需要使用的仪器.
(4)溶质质量分数变大,则可能是溶质质量偏大或溶剂质量偏小,可以分析出可能造成这两个方面错误的原因,进行分析解答即可.
解答 解:(1)16%的氯化钠溶液可以使瘪种子浮起,成熟种子下沉,而水密度较它小,起不到选择作用.
(2)溶质质量=溶液质量×溶质的质量分数,配制80g16%的氯化钠溶液,需氯化钠的质量=80g×16%=12.8g;溶剂质量=溶液质量-溶质质量,则所需水的质量=80g-12.8g=67.2g;水的密度为1g/cm3,则根据V=mρ=495.5g1g/cm3=495.5mL.
(3)配制80g16%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒.
(4)用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大(合理即可).
故答案为:(1)该浓度的溶液可以使瘪种子浮起,成熟种子下沉,而水密度较它小,起不到选择作用;
(2)12.8;67.2;
(3)①③⑤⑥⑩;
(4)量筒量取水时,俯视液面(合理即可).
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤,明确导致溶质质量分数变大的因素等是正确解答本题的关键.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
19.下列各图中,能表示化合物的是( )
| A. | 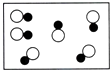 | B. |  | C. |  | D. | 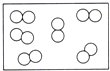 |
20.下列实验方案可行的是( )
| A. | 用观察颜色的方法区别氮气和二氧化硫 | |
| B. | 用过滤的方法除去水中混有的氯化钠 | |
| C. | 用闻气味的方法区别氧气和二氧化碳 | |
| D. | 用蒸发的方法区别海水和蒸馏水 |
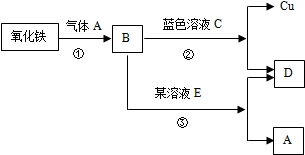
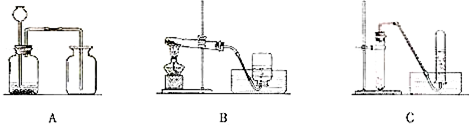
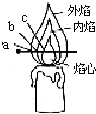 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.