题目内容
 在实验室里进行如图所示的实验,当看到红色变成无色是停止实验.
在实验室里进行如图所示的实验,当看到红色变成无色是停止实验.(1)实验中玻璃棒的作用是
(2)此时能判断烧杯中的溶液一定是中性吗?
(3)为了验证烧杯中稀盐酸是否过量,又继续进行了如下实验.
| 操作 | 现象 | 结论 |
| 取少量烧杯中的液体于试管中,滴加适量的碳酸钠溶液 | 无气泡产生,液体变成 |
(5)若氢氧化钠溶液与稀盐酸恰好完全反应,反应后所得溶液的pH=
考点:中和反应及其应用,酸的化学性质,溶液的酸碱性与pH值的关系,盐的化学性质
专题:常见的酸 酸的通性
分析:(1)实验中玻璃棒搅拌,促进反应的进行.
(2)酚酞遇酸和中性溶液不会变色,可以据此结合盐酸和氢氧化钠溶液的反应来完成解答.
(3)碳酸钠为碱性溶液,且可以和盐酸反应生成气体,可以据此解答该.
足量的氯化钙可以和碳酸盐反应生成白色的碳酸钙沉淀,而使溶液变为中性溶液,可以据此解答该题.
(4)由于借助了酚酞变色来判断反应的发生,所以若证明有新物质生成,还可以将所得溶液进行蒸发,来进行判断,可以据此解答该题.
(5)pH=7,为中性.
(2)酚酞遇酸和中性溶液不会变色,可以据此结合盐酸和氢氧化钠溶液的反应来完成解答.
(3)碳酸钠为碱性溶液,且可以和盐酸反应生成气体,可以据此解答该.
足量的氯化钙可以和碳酸盐反应生成白色的碳酸钙沉淀,而使溶液变为中性溶液,可以据此解答该题.
(4)由于借助了酚酞变色来判断反应的发生,所以若证明有新物质生成,还可以将所得溶液进行蒸发,来进行判断,可以据此解答该题.
(5)pH=7,为中性.
解答:解:(1)实验中玻璃棒的作用是促进反应的进行.
(2)酚酞遇酸和中性溶液不会变色,盐酸和氢氧化钠溶液的反应生成了氯化钠和水,为中性溶液,但是若盐酸过量溶液也会变成无色,所以不能仅仅根据溶液变成无色来判断反应完成.
(3)碳酸钠为碱性溶液,且可以和盐酸反应生成气体,根据题给的实验现象可以知道加入碳酸钠溶液后没产生气体,则说明盐酸和氢氧化钠溶液恰好完全反应,而碳酸钠溶液呈碱性,所以溶液会变成红色.
(4)足量的氯化钙可以和碳酸盐反应生成白色的碳酸钙沉淀,而使溶液变为中性溶液,所以可以观察到溶液中产生白色沉淀,溶液红色消失,该反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(5)若氢氧化钠溶液与稀盐酸恰好完全反应,pH=7,为中性.
故答案为:(1)促进反应的进行;
(2)不能.
(3)
(4)产生白色沉淀,液体由红色又变成无色.
Na2CO3+CaCl2═CaCO3↓+2NaCl.
(5)7.
(2)酚酞遇酸和中性溶液不会变色,盐酸和氢氧化钠溶液的反应生成了氯化钠和水,为中性溶液,但是若盐酸过量溶液也会变成无色,所以不能仅仅根据溶液变成无色来判断反应完成.
(3)碳酸钠为碱性溶液,且可以和盐酸反应生成气体,根据题给的实验现象可以知道加入碳酸钠溶液后没产生气体,则说明盐酸和氢氧化钠溶液恰好完全反应,而碳酸钠溶液呈碱性,所以溶液会变成红色.
(4)足量的氯化钙可以和碳酸盐反应生成白色的碳酸钙沉淀,而使溶液变为中性溶液,所以可以观察到溶液中产生白色沉淀,溶液红色消失,该反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
(5)若氢氧化钠溶液与稀盐酸恰好完全反应,pH=7,为中性.
故答案为:(1)促进反应的进行;
(2)不能.
(3)
| 现象 | 结论 |
| 红色 | 稀盐酸没有过量(或盐酸与氢氧化钠溶液恰好完全反应或溶液为中性) |
Na2CO3+CaCl2═CaCO3↓+2NaCl.
(5)7.
点评:要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景,结合所学的相关知识和技能,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
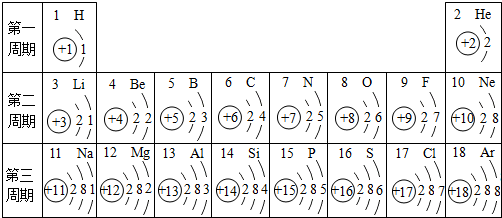
下列关于物质组成的叙述中正确的是( )
| A、纯净物的组成中只含一种元素 |
| B、混合物的组成中肯定含有多种元素 |
| C、不同的物质可以含有相同的元素 |
| D、含氧元素的化合物就是氧化物 |
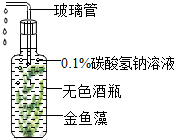 科学兴趣小组设计了如图实验装置.分别用相同强度、不同颜色的光来照射,玻璃管均有水滴排出但数量不等(不考虑温度对水滴排出的影响),表中的是相同时间内排出的水滴数.
科学兴趣小组设计了如图实验装置.分别用相同强度、不同颜色的光来照射,玻璃管均有水滴排出但数量不等(不考虑温度对水滴排出的影响),表中的是相同时间内排出的水滴数.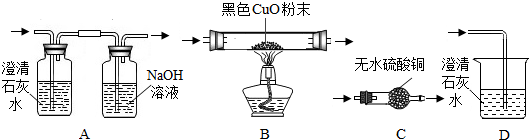
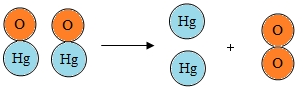 如图是氧化汞分子分解示意图.从示意图中,你能够得出的规律或者结论有:(答出4条即可)
如图是氧化汞分子分解示意图.从示意图中,你能够得出的规律或者结论有:(答出4条即可)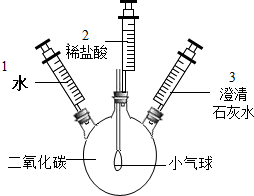 某化学小组的同学在学习《奇妙的二氧化碳》时,设计了如图实验:
某化学小组的同学在学习《奇妙的二氧化碳》时,设计了如图实验: 人体缺乏维生素C(简称“Vc”)就会患坏血病,如图所示为某种“维生素C”药片说明书的一部分.其中,维生素C“化学式”部分残缺,用“C6H8On”表示.
人体缺乏维生素C(简称“Vc”)就会患坏血病,如图所示为某种“维生素C”药片说明书的一部分.其中,维生素C“化学式”部分残缺,用“C6H8On”表示.