题目内容
菱镁矿的主要成分是MgCO3,下列说法正确的是( )
| A、MgCO3的相对分子质量是84 | ||
| B、MgCO3中Mg、C、O元素的质量比是1:1:3 | ||
| C、MgCO3中Mg、C、O的原子个数比是24:12:16 | ||
D、MgCO3中Mg元素的质量分数是
|
分析:A、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
C、根据1个MgCO3分子的构成进行分析判断.
D、根据化合物中元素的质量分数=
×100%,进行分析解答.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
C、根据1个MgCO3分子的构成进行分析判断.
D、根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:A、MgCO3的相对分子质量是24+12+16×3=84,故选项说法正确.
B、MgCO3中Mg、C、O元素的质量比是24:12:(16×3)≠1:1:3,故选项说法错误.
C、1个MgCO3分子是由1个镁原子、1个碳原子和3个氧原子构成的,则MgCO3中Mg、C、O的原子个数比是1:1:3,故选项说法错误.
D、MgCO3中Mg元素的质量分数是
×100%,故选项说法错误.
故选:A.
B、MgCO3中Mg、C、O元素的质量比是24:12:(16×3)≠1:1:3,故选项说法错误.
C、1个MgCO3分子是由1个镁原子、1个碳原子和3个氧原子构成的,则MgCO3中Mg、C、O的原子个数比是1:1:3,故选项说法错误.
D、MgCO3中Mg元素的质量分数是
| 24 |
| 24+12+16×3 |
故选:A.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目

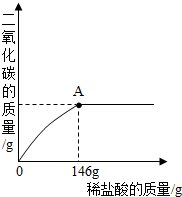 现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:
现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求: C.MgCO3中Mg、C、O的原子个数比是24:12:16
C.MgCO3中Mg、C、O的原子个数比是24:12:16