题目内容
下列盐可以由金属与酸直接反应生成的是
A.NaCl
B.![]()
C.AgCl
D.![]()

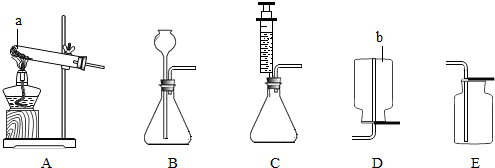
实验台上分类摆放下列药品,兴趣小组欲利用这些药品进行铝和铜性质的探究。

① ② ③ ④ ⑤ ⑥
② Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的 。该变化的化学方程式为
(3)比较铝和铜的金属活动性强弱,可选用上述的 (填序号)试剂进行实验。Ⅱ.将铝片插入硫酸铜溶液中,一段时间后取出,铝片上没有明显变化,其原因是 。
兴趣小组把处理过的铝片放入硫酸铜溶液中,除铝片上有红色金属析出外,还发现有较多气泡产生,于是激发了他们的探究欲望。
【提出问题】该气体是什么呢?
【猜 想】甲同学认为可能是氧气
乙同学认为可能是氢气
丙同学认为可能是二氧化硫
【探究实验】闻该气体的气味,发现没有气味,排除了 同学的猜想。
对余下两种气体猜想进行如下实验:
|
实验步骤 |
现象 |
结论 |
|
|
木条不复燃 |
该气体不是氧气 |
|
收集一试管气体,用拇指堵住管口,移近酒精灯火焰 |
发出轻微的爆鸣声,并产生淡蓝色火焰 |
该气体是 |
【思维拓展】由以上探究实验可以推知,硫酸铜溶液中有 离子参与反应.
【解析】Ⅰ.(1)铝的利用晚于铁、铜是由于金属铝的活动性比铁、铜强,即选项B铝相对活泼;由于活动性较强,其冶炼则会相对比较困难.(2)铝的活动性较强,在常浊下可以与氧气反应生成氧化铝且形成致密的膜覆盖在铝的表面,隔绝金属铝与氧气的接触,防止了进一步氧化.
根据金属活动性的反应规律可进行判断,排在氢前面的金属可以置换出酸中的氢,根据与酸反应的剧烈程度也可以判断金属活动性强弱,活动性强的金属可以把比它活动性弱的金属从其盐溶液中置换出来.
Ⅱ铝在空气中表面易氧化形成氧化铝保护膜,进行有关铝的性质实验需要将其除掉,二氧化硫是有刺激性气味的气体,根据质量守恒定律,化学反应前后,元素的种类不变,氧气能使带火星的木条复燃,检验氢气使用的是收集气体点燃的方法,活泼金属能与酸反应生成氢气.