题目内容
(2011?百色)如图是刚配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算:(1)该硫酸钠溶液中溶剂质量为______ g;
(2)取氯化钡固体样品26g,放入烧杯中加水完全溶解并过滤,往滤液中滴加上述配制的硫酸钠溶液至完全反应,然后过滤、烘干.称得沉淀23.3g.
计算:①该样品中氯化钡的质量分数是多少?
②用去硫酸钠溶液的质量是多少g?

【答案】分析:(1)先求出溶液中溶质的质量,再用溶液的质量-溶质的质量求出溶剂的质量.
(2)①利用氯化钡和硫酸钠反应的化学方程式,根据硫酸钡沉淀的质量求出氯化钡的质量,再根据 ×100%求出样品中氯化钡的质量分数.②根据硫酸钡的质量求出硫酸钠的质量,再根据
×100%求出样品中氯化钡的质量分数.②根据硫酸钡的质量求出硫酸钠的质量,再根据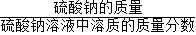 求出所用的硫酸钠溶液的质量.
求出所用的硫酸钠溶液的质量.
解答:(1)溶液中溶质的质量为:500g×10%=50g 则溶剂的质量为:500g-50g=450g
(2)设样品中BaCl2的质量为x,反应用去Na2SO4溶液的质量为y.
BaCl2+Na2SO4=BaSO4↓+2NaCl
208 142 233
x y×10% 23.3g
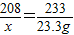 ,x=20.8g
,x=20.8g
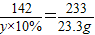 ,y=142g
,y=142g
样品中BaCl2的质量分数为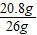 ×100%=80%
×100%=80%
答:样品中BaCl2的质量分数为80%,反应用去Na2SO4溶液的质量为142g.
点评:溶液中溶质的质量分数= ×100%,这个公式要会灵活运用,知道其中的任意两个量,都能求出另外一个量.
×100%,这个公式要会灵活运用,知道其中的任意两个量,都能求出另外一个量.
(2)①利用氯化钡和硫酸钠反应的化学方程式,根据硫酸钡沉淀的质量求出氯化钡的质量,再根据
 ×100%求出样品中氯化钡的质量分数.②根据硫酸钡的质量求出硫酸钠的质量,再根据
×100%求出样品中氯化钡的质量分数.②根据硫酸钡的质量求出硫酸钠的质量,再根据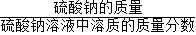 求出所用的硫酸钠溶液的质量.
求出所用的硫酸钠溶液的质量.解答:(1)溶液中溶质的质量为:500g×10%=50g 则溶剂的质量为:500g-50g=450g
(2)设样品中BaCl2的质量为x,反应用去Na2SO4溶液的质量为y.
BaCl2+Na2SO4=BaSO4↓+2NaCl
208 142 233
x y×10% 23.3g
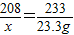 ,x=20.8g
,x=20.8g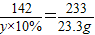 ,y=142g
,y=142g样品中BaCl2的质量分数为
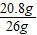 ×100%=80%
×100%=80%答:样品中BaCl2的质量分数为80%,反应用去Na2SO4溶液的质量为142g.
点评:溶液中溶质的质量分数=
 ×100%,这个公式要会灵活运用,知道其中的任意两个量,都能求出另外一个量.
×100%,这个公式要会灵活运用,知道其中的任意两个量,都能求出另外一个量. 
练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
 (2011?百色)(1)如图是A、B、C三种物质的溶解度曲线:
(2011?百色)(1)如图是A、B、C三种物质的溶解度曲线:


