题目内容
11.在实验室里加热氯酸钾和0.5g二氧化锰的混合物制取氧气,完全反应后剩余固体质量为15.4g.请计算:原混合物中氯酸钾的质量.分析 根据质量守恒定律计算生成氯化钾的质量,然后依据化学方程式计算原固体混合物中氯酸钾的质量.
解答 解:反应后生成氯化钾的质量为:15.4g-0.5g=14.9g
设原混合物中氯酸钾的中质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149
x 14.9g
$\frac{245}{x}$=$\frac{149}{14.9g}$
x=24.5g
故答案为:原混合物中氯酸钾的质量是24.5g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
1.下列物质的用途是利用其化学性质的是( )
| A. | 氮气用于磁悬浮列车 | B. | 稀有气体用于制作霓虹灯 | ||
| C. | 过氧化氢用于制取氧气 | D. | 用液态空气制氧气 |
16.关于实验室制取氧气和二氧化碳的说法错误的是( )
| A. | 可共用同种试剂 | B. | 可共用同种发生装置 | ||
| C. | 能用同种收集方法 | D. | 不用酒精灯就可制取两种气体 |
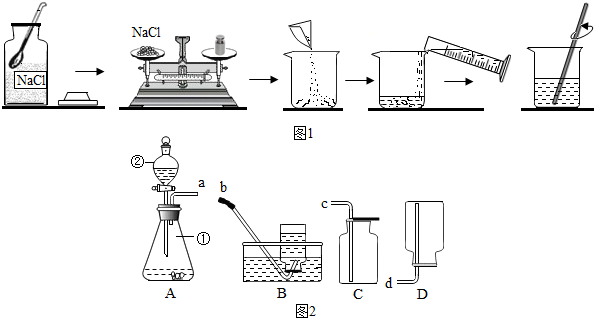
 过氧化氢溶液在二氧化锰催化剂的条件下,分解成氧气和水(装置见如图),分液漏斗可以通过调节活塞控制液体的滴加速度.回答下列问题:
过氧化氢溶液在二氧化锰催化剂的条件下,分解成氧气和水(装置见如图),分液漏斗可以通过调节活塞控制液体的滴加速度.回答下列问题: