题目内容
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。
(1)请写出“湿法炼铜”的化学方程式
。
(2)若用该方法制得铜32 g,反应的铁的质量为 g,若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为 %。
本题考查化学方程式的书写和溶液的有关计算。题目中涉及的化学反应为Fe+CuSO4====Cu+FeSO4,把铜的质量32 g代入化学方程式求出参加反应的铁和硫酸铜的质量,然后据硫酸铜和硫酸铜溶液的质量求出硫酸铜的质量分数。
解:设参加反应铁的质量为x,500 g硫酸铜溶液中硫酸铜的质量为y。
Fe+CuSO4 ==== Cu+FeSO4
56 160 64
x y 32 g
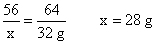
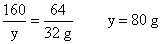
硫酸铜溶液中硫酸铜的质量分数为
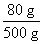 ×100%=16%
×100%=16%
答案:(1)Fe+CuSO4====Cu+FeSO4 (2)28 16

练习册系列答案
相关题目
如下图所示,在a烧杯中盛有浓氨水,在b烧杯中盛有酚酞溶液,有关现象和解释正确的是( )
| 选项 | 现象 | 解释 |
| A | b烧杯溶液变红色 | a中氨分子运动到b中,氨气溶于水,氨水使酚酞溶液变成红色 |
| B | a烧杯溶液变红色 | b中酚酞分子运动到a中,氨气与酚酞反应生成红色物质 |
| C | b烧杯溶液为无色 | a中氨分子没有运动 |
| D | a烧杯溶液为无色 | b中酚酞分子运动到a中,氨水呈中性 |


 含有大量的水
含有大量的水
 机的黑匣子内部保护存储数字信息的内存卡外壳是铝壳,环绕内存卡还有一铝薄层。有关铝的性质的说法中不正确的是( )
机的黑匣子内部保护存储数字信息的内存卡外壳是铝壳,环绕内存卡还有一铝薄层。有关铝的性质的说法中不正确的是( ) 边烧杯中各加入5 g镁和5 g铁,镁和铁全部反应而消失后,天平的指针( )
边烧杯中各加入5 g镁和5 g铁,镁和铁全部反应而消失后,天平的指针( ) 运动
运动