题目内容
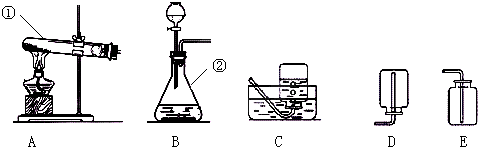
下列实验操作中,能达到实验目的是( )
分析:A、根据鸡蛋壳的主要成分是碳酸钙进行分析判断.
B、根据氧化铜和二氧化锰的溶解性进行分析判断.
C、根据蒸发操作的注意事项进行分析判断.
D、根据pH试纸的使用方法进行分析判断.
B、根据氧化铜和二氧化锰的溶解性进行分析判断.
C、根据蒸发操作的注意事项进行分析判断.
D、根据pH试纸的使用方法进行分析判断.
解答:解:A、鸡蛋壳的主要成分是碳酸钙,不能与食盐水反应,故该实验不能达到实验目的.
B、氧化铜和二氧化锰均不溶于水,也不能与水反应,用水不能区别,故该实验不能达到实验目的.
C、粗盐提纯实验中,蒸发结晶至有较多固体析出时停止加热,故该实验能达到实验目的.
D、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确;故该实验不能达到实验目的.
故选C.
B、氧化铜和二氧化锰均不溶于水,也不能与水反应,用水不能区别,故该实验不能达到实验目的.
C、粗盐提纯实验中,蒸发结晶至有较多固体析出时停止加热,故该实验能达到实验目的.
D、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确;故该实验不能达到实验目的.
故选C.
点评:本题难度不大,掌握碳酸钙的化学性质、蒸发操作、pH试纸的使用方法即可正确解答本题.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
(2010?达州)纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
[交流与反思]若用稀硫酸代替稀盐酸进行实验,是否与猜想二相同?______(填“是”或“否”).
| 猜想 | 实验操作 | 实验现象 | 结论(或化学方程式) |
| 猜想一:Na2CO3溶液显碱性 | 取少量的Na2CO3溶液试管中,滴入2-3滴酚酞试液,振荡 | ______ | 溶液显碱性 |
| 猜想二:能与酸反应 | 取少量的Na2CO3溶液试管中,然后滴加稀盐酸 | 有大量的气泡 | 化学方程式:______ |
| 猜想三:能与Ca(OH)2反应 | 向盛有少量Na2CO3溶液的试管中滴加澄清石灰水 | 出现白色沉淀 | 化学方程式:______ |
| 猜想四:能与氯化钡反应 | ______ | 出现白色沉淀 | Na2CO3+BaCl2=BaCO3↓+2NaCl 反应的基本类型为:______ |