题目内容
向混有少量氧化铜粉末的铁粉中加入足量盐酸,充分反应后,仍有少量固体不溶物.过滤该混合物,滤纸上的残留物是 ,滤液里的溶质是 .
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:氧化铜能和稀盐酸反应生成氯化铜和水,铁能和稀盐酸反应生成氯化亚铁和氢气;
铁能和氯化铜反应生成氯化亚铁和铜.
铁能和氯化铜反应生成氯化亚铁和铜.
解答:解:向混有少量氧化铜粉末的铁粉中加入足量盐酸,充分反应后,仍有少量固体不溶物,该固体不溶物应该是氯化铜和铁反应生成的铜;
如果氧化铜和稀盐酸反应生成的氯化铜完全和铁反应,则滤液里的溶质有氯化亚铁和过量的氯化氢;
如果氧化铜和稀盐酸反应生成的氯化铜没有和铁完全反应,则滤液里的溶质有氯化亚铁、氯化铜和过量的氯化氢.
故填:铜;氯化亚铁、氯化氢,或氯化亚铁、氯化氢、氯化铜.
如果氧化铜和稀盐酸反应生成的氯化铜完全和铁反应,则滤液里的溶质有氯化亚铁和过量的氯化氢;
如果氧化铜和稀盐酸反应生成的氯化铜没有和铁完全反应,则滤液里的溶质有氯化亚铁、氯化铜和过量的氯化氢.
故填:铜;氯化亚铁、氯化氢,或氯化亚铁、氯化氢、氯化铜.
点评:铁既能够和氯化铜反应,也能够和稀盐酸反应,这是判断滤液中是否含有氯化铜的关键.

练习册系列答案
相关题目
某同学在使用托盘天平称取10.5g食盐固体时操作时(1g以下使用游码),错误的将砝码和药品的位置放反了,则该同学称取的食盐固体的真实质量为( )
| A、10.5 g |
| B、9.5 g |
| C、11.0 g |
| D、9.0 g |
在氢气还原氧化铜的实验中,有如下操作步骤:①加热 ②通入氢气 ③停止加热 ④停止通入氢气.下列操作顺序正确的是( )
| A、②①③④ | B、①③②④ |
| C、③①④② | D、①③④② |
下列常见物质中,属于纯净物的是( )
| A、可乐饮料 | B、加碘食盐 |
| C、蒸馏水 | D、调味食醋 |
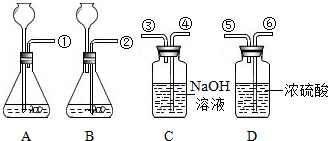
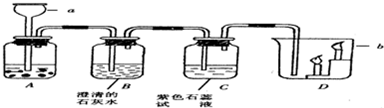
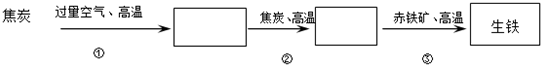
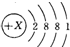 ,则x=
,则x=