题目内容
已知R3N2的相对分子质量为100,则R的相对原子质量为________;R3N2中氮元素的质量分数为________.
24 28%
分析:根据相对分子质量为组成分子的各原子的相对原子质量之和,化合物中元素的质量分数=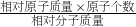 ×100%,进行分析解答.
×100%,进行分析解答.
解答:已知R3N2的相对分子质量为100,设R的相对原子质量为x,则3x+14×2=100,x=24.
R3N2中氮元素的质量分数为 100%=28%.
100%=28%.
故答案为:24;28%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
分析:根据相对分子质量为组成分子的各原子的相对原子质量之和,化合物中元素的质量分数=
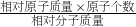 ×100%,进行分析解答.
×100%,进行分析解答.解答:已知R3N2的相对分子质量为100,设R的相对原子质量为x,则3x+14×2=100,x=24.
R3N2中氮元素的质量分数为
 100%=28%.
100%=28%.故答案为:24;28%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
化学兴趣小组同学在实验室配制石灰水时,小明同学将两药匙熟石灰样品放入小烧杯中,加入一定量的蒸馏水,充分搅拌后发现烧杯底部仍有不溶性的固体,于是他认为熟石灰样品已经变质.小艳同学不同意他的判断,你认为小艳同学的理由是________.同学们针对该熟石灰样品的成分展开了讨论,请你参与讨论并完成实验报告.
【提出问题】熟石灰样品的主要充分是什么?
【作出猜想】
甲同学猜想是Ca(OH)2;
乙同学猜想是CaCO3
你认为是________.
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤. 向滤液中加入适量的________溶液; 向滤出固体中加入适量________溶液. | ________; ________. | 猜想正确 |
【我会计算】同学们为了测定某敞口放置一段时间的熟石灰样品中Ca(OH)2的含量(杂质为CaCO3),取17.4g该样品,加入100g盐酸,恰好完全反应,产生气体的质量为4.4g,试计算试样中Ca(OH)2的质量分数.
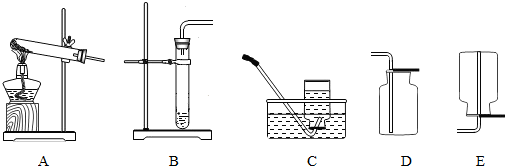





 用右图装置加热高锰酸钾制取氧气,请回答:
用右图装置加热高锰酸钾制取氧气,请回答: 如图是世界无车日的宣传画,我国许多城市开展了“无车日”活动,市区的主要街道禁行机动车辆,有效地减少了有害气体排放.下列物质中,属于有害气体,必须减少排放的是________
如图是世界无车日的宣传画,我国许多城市开展了“无车日”活动,市区的主要街道禁行机动车辆,有效地减少了有害气体排放.下列物质中,属于有害气体,必须减少排放的是________