题目内容
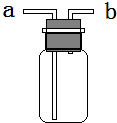 如图所示装置被称为“洗气瓶”,洗气瓶又叫“万能瓶”.
如图所示装置被称为“洗气瓶”,洗气瓶又叫“万能瓶”.(1)用排空气法收集一瓶氢气(氢气密度比空气小),氢气从
b
b
端(填“a”或“b”,下同)进入;(2)用排水法收集一瓶氧气,将洗气瓶充满水,氧气从
b
b
端进入;(3)收集50ml氢气,将洗气瓶充满水,在
a
a
端放置一只50mL量筒
50mL量筒
,氢气从另一端端进入;(4)除去一氧化碳中混有的少量二氧化碳,在洗气瓶内放入一定量
氢氧化钠溶液
氢氧化钠溶液
,混合气体从a
a
端进入.…“万能瓶”当然还有很多用途,这里不再多说.
分析:根据装置的特点结合常用气体的收集方法进行分析解答本题.
解答:解:(1)用排空气法收集一瓶氢气(氢气密度比空气小),因为氢气的密度比空气小,因此氢气从b端进入;
(2)用排水法收集一瓶氧气,将洗气瓶充满水,因为氧气的密度比水小,因此氧气从b端进入;
(3)收集50ml氢气,将洗气瓶充满水,因氢气的密度比水小,因此气体应从b端进入,水从a端排出,所以应在a端放置一只50mL量筒;
(4)除去一氧化碳中混有的少量二氧化碳,因为二氧化碳和氢氧化钠溶液反应而一氧化碳不会和氢氧化钠溶液反应,因此可在洗气瓶内放入一定量氢氧化钠溶液,又因为二氧化碳和一氧化碳气体的密度比氢氧化钠溶液的小,因此混合气体应从a端进入,从b端导出.
故答案为:(1)b;(2)b;(3)a;50mL量筒;(4)氢氧化钠溶液;a.
(2)用排水法收集一瓶氧气,将洗气瓶充满水,因为氧气的密度比水小,因此氧气从b端进入;
(3)收集50ml氢气,将洗气瓶充满水,因氢气的密度比水小,因此气体应从b端进入,水从a端排出,所以应在a端放置一只50mL量筒;
(4)除去一氧化碳中混有的少量二氧化碳,因为二氧化碳和氢氧化钠溶液反应而一氧化碳不会和氢氧化钠溶液反应,因此可在洗气瓶内放入一定量氢氧化钠溶液,又因为二氧化碳和一氧化碳气体的密度比氢氧化钠溶液的小,因此混合气体应从a端进入,从b端导出.
故答案为:(1)b;(2)b;(3)a;50mL量筒;(4)氢氧化钠溶液;a.
点评:本题考查学生根据题意和常用气体的收集方法进行分析解题的能力.

练习册系列答案
相关题目
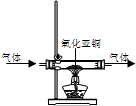 Cu可以形成化合价为+2和+1的化合物,其中+1价化合物称为亚铜化合物.
Cu可以形成化合价为+2和+1的化合物,其中+1价化合物称为亚铜化合物.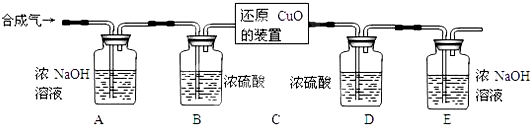
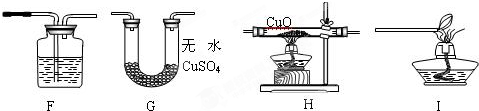
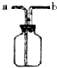 如图所示装置在化学实验室中常被称为“万能瓶”.
如图所示装置在化学实验室中常被称为“万能瓶”.