题目内容
13.根据下列装置图,回答有关问题:
(1)图中标有a的仪器名称是试管.
(2)实验室用氯酸钾制取氧气,应选用的发生装置是A(填字母),反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,收集装置为C(填字母),验满的方法为将燃着的木条放在集气瓶口,木条熄灭,则证明已满.将产生的气体导入澄清的石灰水结果未变浑浊可能的原因是石灰水变质(二氧化碳中混有氯化氢气体)等.
(4)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,然后将其灼烧(2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO).改进后的发生装置如图F所示(已略去夹持装置).
①铜丝绕成螺旋状的作用是B(填字母).
A.收集到更多的O2 B.加快反应速率 C.没有影响
②与装置B比较,改进后装置的优点是可随时控制反应的进行或停止.
分析 (1)要熟练掌握各种仪器的名称和用途;
(2)实验室用氯酸钾制取氧气时需要加热解答;
(3)实验室可以用石灰石和稀盐酸反应制取二氧化碳,二氧化碳易溶于水,密度比空气大解答,
解答 解:(1)①是试管.
(2)实验室用氯酸钾制取氧气时需要加热,应该用A装置;氧气不易溶于水,密度比空气大,可以用向上排空气法或排水法收集.故填:A、C或E.
氯酸钾在催化剂的作用下,受热分解能生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室可用B装置制取二氧化碳气体,试剂是石灰石和稀盐酸,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.二氧化碳易溶于水,密度比空气大,可以用向上排空气法收集;验满的方法为:将燃着的木条放在集气瓶口,木条熄灭,则证明已满;将制取的二氧化碳气体通入盛有澄清的石灰水中,澄清的石灰水没有变浑浊,可能的原因是:盐酸浓度大或石灰水浓度太稀或变质等;
(4)①将铜丝绕成螺旋状,增大了与反应物的接触面积,加快了反应的速率,故选:B;
②改进后的装置,通过抽动铜丝来控制反应的发生和停止;故填:可随时控制反应的进行或停止;
答案:
(1)试管;
(2)A;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;C;将燃着的木条放在集气瓶口,木条熄灭,则证明已满;石灰水变质(二氧化碳中混有氯化氢气体)等;
(4)①B;②可随时控制反应的进行或停止;
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
3.属于物理变化的是( )
| A. | 食物腐败 | B. | 木炭燃烧 | C. | 玻璃破碎 | D. | 动物呼吸 |
4.下列化学方程式书写及基本反应类型都正确的是( )
| A. | 木炭在空气中燃烧:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;化合反应 | |
| B. | 甲烷燃烧:CH4+ 2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O;化合反应 | |
| C. | 加热高锰酸钾制取氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+MnO2+O2↑;分解反应 | |
| D. | 加热铜丝:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;氧化反应 |
18.向下列物质中加入足量的水,充分搅拌,能形成溶液的是( )
| A. | 冰块 | B. | 白糖 | C. | 面粉 | D. | 食用油 |
5.如表各选项中,解释与事实不吻合的是( )
| 选项 | 事实 | 解释 |
| A | 液氧和氧气都能使带火星的木条复燃 | 同种分子的化学性质相同 |
| B | 酒精做温度计的填充物 | 酒精分子的体积受热变大,遇冷变小 |
| C | 金刚石很坚硬,而石墨却很软 | 碳原子的排列不同 |
| D | 食物变质 | 分子本身发生了变化 |
| A. | A | B. | B | C. | C | D. | D |
3.每年的5月12日是我国的“防灾减灾日”.下列有关做法或说法不合理的是( )
| A. | 火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打火警电话119 | |
| B. | 扑灭森林火灾,可将大火蔓延路线前的一片树木砍掉,形成隔离带 | |
| C. | 在油库、面粉厂、纺织厂等场所,要严禁烟火 | |
| D. | 只要温度达到着火点,可燃物就一定会燃烧 |
 用如图所示装置探究可燃物的燃烧条件.实验过程如下:
用如图所示装置探究可燃物的燃烧条件.实验过程如下: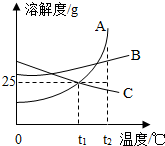 图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题:
图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题: 如图所示,将充满二氧化碳的试管倒扣在滴有紫色石蕊的蒸馏水中.
如图所示,将充满二氧化碳的试管倒扣在滴有紫色石蕊的蒸馏水中.