题目内容
除去CaCl2固体中混有的CaCO3 杂质,下列各组中选用试剂,操作方法都正确的是
- A.加水,搅拌,过滤,烘干
- B.加NaCl,搅拌,过滤,蒸发
- C.加适量稀硫酸,搅拌,蒸发
- D.加适量稀盐酸,搅拌,蒸发
D
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:A、CaCl2固体易溶于水,CaCO3难溶于水,可采取加水溶解、搅拌、过滤、蒸发的方法进行分离除杂,故选项所采取的方法错误.
B、NaC不能与CaCl2固体、CaCO3反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、CaCO3能与稀硫酸反应生成硫酸钙、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钙,不符合除杂原则,故选项所采取的方法错误.
D、CaCO3能与稀盐酸反应生成氯化钙、水和二氧化碳,再搅拌、蒸发,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选D.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:A、CaCl2固体易溶于水,CaCO3难溶于水,可采取加水溶解、搅拌、过滤、蒸发的方法进行分离除杂,故选项所采取的方法错误.
B、NaC不能与CaCl2固体、CaCO3反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、CaCO3能与稀硫酸反应生成硫酸钙、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钙,不符合除杂原则,故选项所采取的方法错误.
D、CaCO3能与稀盐酸反应生成氯化钙、水和二氧化碳,再搅拌、蒸发,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选D.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
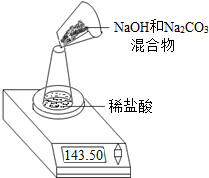 某NaOH固体中含有Na2CO3.老师安排第一小组做除去NaOH固体中Na2CO3的实验.第二、第三小组同学做测定该固体混合物中Na2CO3质量分数的实验.
某NaOH固体中含有Na2CO3.老师安排第一小组做除去NaOH固体中Na2CO3的实验.第二、第三小组同学做测定该固体混合物中Na2CO3质量分数的实验.Ⅰ,第一小组的同学取一定量的该固体溶于水,得到混合溶液,为了除去溶液中的Na2CO3杂质,甲、乙、丙、丁四位同学分别选择下列试剂进行实验.其中合理的是
甲:适量稀盐酸 乙:过量KOH溶液 丙:适量Ba(OH)2溶液 丁:适量CaCl2溶液.
Ⅱ,第二小组利用左下图装置测定NaOH和Na2CO3的混合物中Na2CO3的质量分数,用电子天平称量数据如下表:则混合物中Na2CO3的质量分数为
| 称量项目 | 质量(g) |
| NaOH和Na2CO3的混合物 | 9.30 |
| 锥形瓶+稀盐酸质量(过量) | 141.20 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合物(反应开始后15秒) | 148.50 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合物(反应开始后35秒) | 148.30 |
| 锥形瓶+稀盐酸质量+全部NaOH和Na2CO3的混合物(反应开始后55秒) | 148.30 |

(1)A是
(2)B操作的名称是
(3)混合物中Na2CO3的质量分数为
