题目内容
用Na2CO3、CaCO3和H2O为原料来制取NaOH,所发生的化学反应中不包括( )A.化合反应
B.置换反应
C.分解反应
D.复分解反应
【答案】分析:由转化过程中涉及的反应进行分析判断.
解答:解:用碳酸钙作原料可以通过下列反应实现转化:
①CaCO3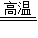 CaO+CO2↑;
CaO+CO2↑;
②CaO+H2O═Ca(OH)2;
③Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
上述反应分别属于分解反应、化合反应、复分解反应.发生的化学反应中不包括置换反应.
故选B.
点评:明确四种基本反应类型的特点:分解反应一变多,化合反应多变一,置换反应是单质和化合物生成另一种单质和另一种化合物,复分解反应是两种化合物交换成分,化合价不变.
解答:解:用碳酸钙作原料可以通过下列反应实现转化:
①CaCO3
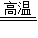 CaO+CO2↑;
CaO+CO2↑;②CaO+H2O═Ca(OH)2;
③Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
上述反应分别属于分解反应、化合反应、复分解反应.发生的化学反应中不包括置换反应.
故选B.
点评:明确四种基本反应类型的特点:分解反应一变多,化合反应多变一,置换反应是单质和化合物生成另一种单质和另一种化合物,复分解反应是两种化合物交换成分,化合价不变.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 21、若每一个圆表示一种物质(图1),用两圆相切表示两种物质可以发生化学反应,“→”表示两物质间的转化关系(其他相关反应物、生成物和反应条件已省略)请回答下列问题:
21、若每一个圆表示一种物质(图1),用两圆相切表示两种物质可以发生化学反应,“→”表示两物质间的转化关系(其他相关反应物、生成物和反应条件已省略)请回答下列问题:
