题目内容
为探究CO2的化学性质需要制取并收集干燥的CO2,以下是老师提供的一些实验装置:

(1)实验室制取CO2的化学方程式为_________________________________________。
(2)浓硫酸 的作用是____________________,收集装置为________(填字母)。
的作用是____________________,收集装置为________(填字母)。
(3)化学课上,李芹同学将燃烧的钠迅速伸入盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出问题】 黑色颗粒和白色物质可能是什么呢?
【进行猜 想】 你认为黑色颗粒是________,小明认为白色物质是氧化钠,小艺认为是碳酸钠,小亮认为是氧化钠和碳酸钠的混合物,小华认为是氢氧化钠。
想】 你认为黑色颗粒是________,小明认为白色物质是氧化钠,小艺认为是碳酸钠,小亮认为是氧化钠和碳酸钠的混合物,小华认为是氢氧化钠。
李芹同学认为小华的猜想是错误的,其理由是__________________________________。
【查阅资料】 CaCl2+Na2CO3===CaCO3↓+2NaCl,氧化钠为白色粉末,溶于水生成氢氧化钠。
【实验探究】 李芹同学对白色物质进行实验探究。
实验方案1:取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,向其中加入无色酚酞溶液,观察到溶液变成红色。结论:白色物质为氧化钠。
实验方案2:取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液,出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞溶液,无明显现象出现。结论:白色物质为________。
【反思评价】 小娟同学认为实验方案1得出的结论不正确,其理由是____________。
【得出结论】 钠在二氧化碳中燃烧的化学方程式为____________________________。
答案:(1)CaCO3+2HCl===CaCl2+H2O+CO2↑
(2)吸水 B
(3)炭黑 反应物中无氢元素 Na2CO3 Na2CO3溶液也能使酚酞溶液变红 4Na+3CO2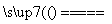 2Na2CO3+C
2Na2CO3+C
解析:(1)石灰石中的CaCO3与盐酸反应生成CaCl2、H2O和CO2。
(2)浓硫酸具有吸水性,可干燥CO2;CO2密度大于空气且溶于水,故用向上排空气法收集CO2。
(3)反应物是CO2和Na,故产生的黑色颗粒一定是炭黑;由于反应物中没有氢(H)元素,故不可能生成NaOH;根据信息CaCl2和Na2CO3反应生成白色沉淀,且反应后溶液不显碱性,则推知白色物质一定有Na2CO3,而没有Na2O;方案1中若白色物质不是Na2O,而是Na2CO3,其溶液也显碱性,也能使无色酚酞溶液变红。

 阅读快车系列答案
阅读快车系列答案