题目内容
10.为了探究“水的净化”过程,某实验小组从护城河中取了水样,观察到:A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行过滤(填操作名称),
①请你帮他们选出操作所必须的仪器:铁架台、烧杯、漏斗、玻璃棒.
②玻璃棒的作用是引流,漏斗下端要紧靠烧杯内壁,原因是防止液体溅出.
③除去固体小颗粒,再向滤液中加入活性炭,利用其吸附性除去水样中的颜色和异味,该过程属于物理变化(填“物理”或“化学”).
(2)加入氯气杀菌消毒,得到自来水,净化后得到的水属于混合物(填“纯净物”或“混合物”).
(3)地球表面约有71%被水覆盖,但可供人类利用的淡水总量却不足1%.爱护水资源是每个公民的责任和义务.下列行为属于节约用水的是D(填序号)
A.洗澡擦香皂时不关上喷头 B.不间断放水刷牙
C.用自来水不断的为西瓜冲水降温 D.用洗衣水冲厕所.
分析 根据已有的水的净化的知识进行分析解答,根据过滤操作的仪器、注意事项解答;活性炭具有吸附性,根据节约用水的措施解答即可.
解答 解:(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行过滤操作,除去不溶性固体杂质,故填:过滤;
①过滤操作所必须的仪器有:铁架台、烧杯、漏斗、玻璃棒,故填:铁架台;烧杯;漏斗;玻璃棒.
②玻璃棒的作用是引流,漏斗下端要紧靠烧杯内壁,是为了防止液体溅出,故填:引流;防止液体溅出.
③除去固体小颗粒,再向滤液中加入活性炭,利用其吸附性除去水样中的颜色和异味,该过程没有生成新的物质,属于物理变,故填:吸附;物理.
(2)加入氯气杀菌消毒,得到自来水,净化后得到的水含有可溶性杂质,属于混合物,故填:混合物.
(3)A.洗澡擦香皂时不关上喷头会造成水的浪费;
B.不间断放水刷牙会造成水的浪费;
C.用自来水不断的为西瓜冲水降温会造成水的浪费;
D.用洗衣水冲厕所能节约用水;
故填:D.
点评 掌握水的净化的方法是正确解答本题的关键.

练习册系列答案
相关题目
1.关于相对原子质量的叙述:
①相对原子质量就是一个原子的质量;
②相对原子质量是一个碳原子质量的$\frac{1}{12}$
③相对原子质量是原子的相对质量,是一个比值;
④相对原子质量的单位是“千克”;
⑤相对原子质量近似值为质子数和中子数之和;
其中正确的是( )
①相对原子质量就是一个原子的质量;
②相对原子质量是一个碳原子质量的$\frac{1}{12}$
③相对原子质量是原子的相对质量,是一个比值;
④相对原子质量的单位是“千克”;
⑤相对原子质量近似值为质子数和中子数之和;
其中正确的是( )
| A. | ③④⑤ | B. | ④⑤ | C. | ③⑤ | D. | ②③⑤ |
18.下列说法正确的是( )
| A. | 饱和溶液就是无论条件如何变化都不能溶解某种溶质的溶液 | |
| B. | 饱和溶液是指很浓的溶液,不饱和溶液是指比较稀的溶液 | |
| C. | 饱和溶液不会变成不饱和溶液,不饱和溶液也不会变成饱和溶液 | |
| D. | 在一定温度下往20g水中放入一些蔗糖,充分搅拌后仍有固体蔗糖剩余,这时的蔗糖溶液时饱和溶液 |
5.化学新教材加大了化学实验探究的力度,提高了同学们动手实验的能力,如图所示基本的实验操作不正确的是( )
| A. |  液体体积读数 | B. |  熄灭酒精灯 | C. | 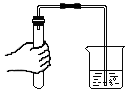 检查气密性 | D. |  滴加液体 |
15.填写如表,已知每个电子的质量约为每个质子(或中子)质量的$\frac{1}{1836}$,通过下表,不仅可以总结出“在原子里质子数等于电子数”,还能总结出:
(1)质子数不一定等于中子数
(2)有些原子没有中子
(3)不同的原子质子数不同.
| 原子种类 | 氢 | 碳 | 氧 | 钠 | 铁 |
| 质子数 | 1 | 6 | 8 | 11 | 26 |
| 中子数 | 0 | 6 | 8 | 12 | 30 |
| 核外电子数 | 1 | 6 | 8 | 11 | 26 |
(2)有些原子没有中子
(3)不同的原子质子数不同.
2.四位同学分别归纳出下列结论:①氧气在一定条件下可转化成臭氧,该变化肯定是物理变化;②物质变色了则一定发生了化学变化;③爆炸不一定是化学变化;④某固态物质在一定条件下观察到放出气体,则一定是发生了化学变化.其中正确的是( )
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ③ |
2.水是重要资源,下列说法正确的是( )
| A. | 过滤和煮沸均能使硬水转化为软水 | |
| B. | 活性炭的吸附作用可使海水转化为淡水 | |
| C. | 电解水得到的氢气和氧气的质量比为2:1 | |
| D. | 水通过“三态”变化在自然界中循环 |
3.下列反应既不属于分解反应,也不属于化合反应的是( )
| A. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | B. | 2Cu+H2O+CO2+O2═Cu2(OH)2CO3 | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+4NO2↑+O2↑ |
