题目内容
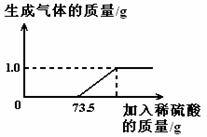
某兴趣小组对生锈废铁锅中铁的含量进行了测定。生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应)。兴趣小组的同学称取36g废铁锅片放入容器中,缓慢加入20%的稀硫酸,直到反应恰好完成(假设硫酸先与表面的铁锈发生反应,铁只 与硫酸反应),实验数据如图所示。
与硫酸反应),实验数据如图所示。
(1)从化学元素与人体健康的角度考虑,我们应选用铁锅还是铝锅 ,原因是
。
(2)废铁锅片中铁单质的质量分数为 (结果保留到0.1%)
 (3)所得溶液中所含溶质的化学式为 ,计算溶液中硫酸铁的质量(要求写出计算过程)。
(3)所得溶液中所含溶质的化学式为 ,计算溶液中硫酸铁的质量(要求写出计算过程)。
(1)铁锅(1分);铁是人体必需的微量元素,而铝是不必需元素,而且铝元素对人体有害(1分)(2)77.8%;84.8%(1分)(3)Fe2(SO4)3、FeSO4(1分)(缺一个或有错项不得分)
解:设生成Fe2(SO4)3的质量为x
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O (1分)
3×98 400
73.5g×20% x (1分)
x= 20g (1分)
答:溶液中硫酸铁的质量为20g。

练习册系列答案
相关题目
 (2012?东营)某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.
(2012?东营)某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示. 某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.
某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.

