题目内容
17.“空气+水=汽油”,这个简单的公式需要首先从空气中提取二氧化碳,把二氧化碳和氢氧化钠溶液混合发生反应,生成碳酸钠和水,其次,通过特殊设备对碳酸钠溶液进行电解,生产出纯净的二氧化碳气体,第三,通过电解水蒸气提取氢气,第四,在反应炉内将二氧化碳和氢气进行有机合成,制造出甲醇(CH3OH).最终甲醇经汽油燃料反应器“变身”为汽油.试写出第三及第四步中发生反应的方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;CO2+3H2═CH3OH+H2O.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:第三步:通过电解水蒸气提取氢气,同时生成氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
第四步:在反应炉内将二氧化碳和氢气进行有机合成,制造出甲醇(CH3OH),同时还应生成水,反应的化学方程式为:CO2+3H2═CH3OH+H2O.
故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;CO2+3H2═CH3OH+H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
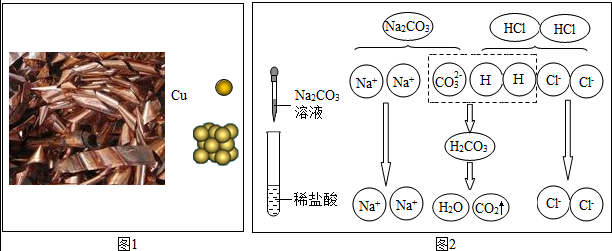
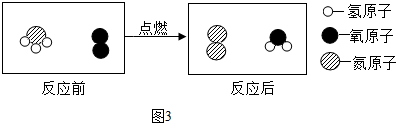
8.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如表格及图2.请根据有关信息回答问题.

(1)a的数值为25.
(2)求该品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数.(写出计算过程,计算结果保留一位小数)
| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |

(1)a的数值为25.
(2)求该品牌补钙药剂中CaCO3的质量分数.
(3)求该盐酸中溶质的质量分数.(写出计算过程,计算结果保留一位小数)
5.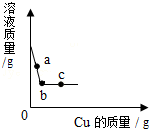 向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
 向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )| A. | a点对应溶液中的溶质有2种 | B. | b点对应固体只有Ag | ||
| C. | b~c段对应溶液中含有AgNO3 | D. | c点时反应已经停止 |
12.小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请把以下探究过程补充完全.
【作出猜想】:1.Cr>Fe>Cu 2. Fe>Cu>Cr 3.Fe>Cr>Cu.
【查阅资料】(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种浓度的稀硫酸.
【结论与解释】(1)小聪得到的结论是猜想I正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜.
【知识运用】如果将光洁的铬片投入到CuSO4溶液中,反应的现象为铬片表面有红色固体生成.反应的化学方程式为Cr+CuSO4=Cu+CrSO4.
【作出猜想】:1.Cr>Fe>Cu 2. Fe>Cu>Cr 3.Fe>Cr>Cu.
【查阅资料】(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种浓度的稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  |  | 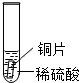 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜.
【知识运用】如果将光洁的铬片投入到CuSO4溶液中,反应的现象为铬片表面有红色固体生成.反应的化学方程式为Cr+CuSO4=Cu+CrSO4.
8.从防火、灭火、自救等安全知识判断,下列做法错误的是( )
| A. |  用明火检验燃气是否泄漏 | B. |  炒菜时油锅着火用锅盖盖灭 | ||
| C. |  室内着火时不急于打开门窗 | D. |  发生火灾逃生时用湿毛巾捂住口鼻 |
5.没有化学科学的发展,就没有今日丰富多彩的世界.下列事实不是化学科学研究的主要内容是( )
| A. | 某种金属矿物的产地 | B. | 功能材料的制造 | ||
| C. | 农药化肥的研制 | D. | 能源的开发和利用 |
6.饮料中的果味大多来自酯类.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂.有关叙述中正确的是( )
| A. | 丁酸乙酯是由20个原子构成的 | |
| B. | 丁酸乙酯的相对分子质量为116 | |
| C. | 丁酸乙酯中碳元素质量分数为27.6% | |
| D. | 丁酸乙酯中碳、氢、氧的质量比为6:12:2 |