题目内容
有一种由氯化钠和硝酸钠组成的固体混合物12.35g,加入27g水使其完全溶解,滴入硝酸银溶液75g,恰好完全反应,生成氯化银沉淀14.35g.计算:
(1)混合物中,氯化钠的质量。
(2)反应后滤液中溶质的质量分数。
【答案】
(1)x=5.85g (2)15%
【解析】
试题分析:由沉淀质量根据氯化钠与硝酸银反应的化学方程式可以计算出混合物中氯化钠的质量和生成硝酸钠的质量,进而计算出反应后滤液中溶质的质量分数。
解:设固体混合物中氯化钠的质量为x,反应后生成硝酸钠的质量为y
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5 85
x 14.35g y
(1)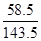 =
=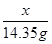 ÷
÷
解得x=5.85g
(2)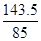 =
=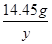
解得y=8.5g
反应后滤液中溶质的质量分数为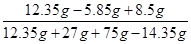 ×100%=15%
×100%=15%
答:(1)混合物中氯化钠的质量为5.85g。
(2)反应后滤液中溶质的质量分数为15%。
考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目