题目内容
现有硫酸和硫酸铜的混合溶液124.9 g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀的质量与所加入的氢氧化钠溶液的质量关系如右图所示。求:
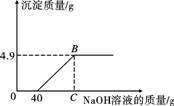
(1)恰好生成最大沉淀量时所加入的氢氧化钠溶液的总质量为____g;
(2)恰好生成最大沉淀量时所得溶液中溶质的质量分数。
80
 解:设与硫酸铜溶液反应的氢氧化钠溶液的质量为x,生成的硫酸钠的质量为y。
解:设与硫酸铜溶液反应的氢氧化钠溶液的质量为x,生成的硫酸钠的质量为y。
CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4
Cu(OH)2↓+Na2SO4
80 98 142
x×10% 4.9 g y
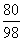 =
=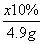 x=40 g
x=40 g
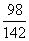 =
=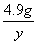 y=7.1 g
y=7.1 g
(1)依图可知,与H2SO4反应消耗氢氧化钠溶液为40 g,故生成最大沉淀量时,加入的氢氧化钠溶液总质量为:40 g+40 g=80 g。
(2)设NaOH与H2SO4反应生成的Na2SO4质量为z。
2NaOH+H2SO4===N a2SO4+H2O
a2SO4+H2O
80 142
40×10% z
 =
=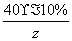 z=7.1 g
z=7.1 g
溶液中Na2SO4的质量分数= ×100%=7.1%
×100%=7.1%

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目

 Cu+H2O 3CO+Fe2O3
Cu+H2O 3CO+Fe2O3 2Fe+3CO2 C+O2
2Fe+3CO2 C+O2 O、C)作还原剂时,所含元素中,一定有元素的化合价在反应后__ __(填“
O、C)作还原剂时,所含元素中,一定有元素的化合价在反应后__ __(填“ 升高”“降低”或“不变”)。
升高”“降低”或“不变”)。
 浊,生成白色沉淀A。D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀。请回答:
浊,生成白色沉淀A。D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀。请回答:
 品,可由A、B两种溶液发生中和反应得到,则A与B反应的化学方程式为_ _。
品,可由A、B两种溶液发生中和反应得到,则A与B反应的化学方程式为_ _。