题目内容
 如图所示是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
如图所示是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH______7.
(2)根据曲线判断,该反应是将什么溶液滴入什么溶液中?______理由是______.
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为______、______(写化学式).
解:(1)氢氧化钠和氯化氢是强电解质,所以生成的氯化钠不水解,当恰好反应时,溶液中电荷守恒C(Na+)+c(H+)=c(Cl-)+c(OH-),因为氯化钠不水解,所以C(Na+)=c(Cl-),则(H+)=c(OH-),溶液呈中性,则pH=7,故答案为:等于;
(2)根据曲线中pH和氢氧化钠体积的关系,当氢氧化钠的体积为0时溶液呈酸性,随着滴入溶液的增加,溶液的pH增大,所以该反应是将氢氧化钠向盐酸中滴加;
(3)当滴入溶液的体积为5mL时,所得溶液呈酸性,因为氯化钠溶液呈中性,则混合溶液中呈酸性的溶质是盐酸,所以当滴入溶液的体积为5mL时,所得溶液中的溶质为NaCl、HCl.
故答案为:(1)等于(或=);(2)氢氧化钠溶液滴入盐酸中;溶液的PH由小于7到大于7;(3)NaCl;HCl.
分析:(1)氢氧化钠和氯化氢是强电解质,所以生成的氯化钠不水解,当恰好反应时,根据电荷守恒判断溶液的pH;
(2)根据曲线中pH和氢氧化钠体积的关系判断;
(3)当滴入溶液的体积为15mL时,所得溶液呈碱性,根据氯化钠、氢氧化钠和盐酸的酸碱性判断溶液中的溶质,石蕊试液遇碱变蓝色
点评:本题考查酸碱中和滴定,正确分析图象是解本题关键,难度不大.
(2)根据曲线中pH和氢氧化钠体积的关系,当氢氧化钠的体积为0时溶液呈酸性,随着滴入溶液的增加,溶液的pH增大,所以该反应是将氢氧化钠向盐酸中滴加;
(3)当滴入溶液的体积为5mL时,所得溶液呈酸性,因为氯化钠溶液呈中性,则混合溶液中呈酸性的溶质是盐酸,所以当滴入溶液的体积为5mL时,所得溶液中的溶质为NaCl、HCl.
故答案为:(1)等于(或=);(2)氢氧化钠溶液滴入盐酸中;溶液的PH由小于7到大于7;(3)NaCl;HCl.
分析:(1)氢氧化钠和氯化氢是强电解质,所以生成的氯化钠不水解,当恰好反应时,根据电荷守恒判断溶液的pH;
(2)根据曲线中pH和氢氧化钠体积的关系判断;
(3)当滴入溶液的体积为15mL时,所得溶液呈碱性,根据氯化钠、氢氧化钠和盐酸的酸碱性判断溶液中的溶质,石蕊试液遇碱变蓝色
点评:本题考查酸碱中和滴定,正确分析图象是解本题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


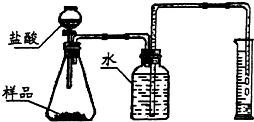 某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分熔化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题:
某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分熔化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题: (2013?川汇区三模)如图所示是氢氧化钠的溶解度曲线,请回答下列问题:
(2013?川汇区三模)如图所示是氢氧化钠的溶解度曲线,请回答下列问题: