题目内容
15.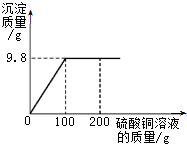 将一定质量的氢氧化钠完全溶于水形成溶液,向其中加入一定质量16%的硫酸铜溶液,测得所得沉淀与加入硫酸铜溶液质量的关系如图20所示.
将一定质量的氢氧化钠完全溶于水形成溶液,向其中加入一定质量16%的硫酸铜溶液,测得所得沉淀与加入硫酸铜溶液质量的关系如图20所示.(1)反应后产生沉淀的质量是9.8g.
(2)恰好完全反应时,测得所得溶液质量为142g,计算此时所得溶液的溶质质量分数.
分析 (1)根据如图信息可知,反应生成的沉淀质量;
(2)根据沉淀的质量可以计算出生成的硫酸钠的质量,利用溶质质量分数公式即可解答.
解答 解:
(1)根据如图可知,反应生成的沉淀质量为9.8g;
(2)设反应生成Na2SO4的质量为x.
2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
98 142
9.8g x
$\frac{98}{9.8g}=\frac{142}{x}$
x=14.2 g
反应后溶液的溶质质量分数为:$\frac{14.2g}{142g}$×100%=10%
答案:
(1)9.8;
(2)反应后溶液的溶质质量分数10%
点评 对反应的图象中曲线进行分析,该曲线的起点表示硫酸被完全反应、折点表示硫酸铜与氢氧化钠恰好完全反应.

练习册系列答案
相关题目
5.下列图示实验操作中正确的是( )
| A. |  倾倒液体 | B. |  量筒读数 | ||
| C. |  称量食盐 | D. |  检查装置的气密性 |
6.如图是某化学反应的微观示意图,下列说法不正确的是( )


| A. | 参加反应的两种反应物的分子个数比为3:1 | |
| B. | 此反应是化合反应 | |
| C. | 此反应过程中原子的种类和数目没有发生变化 | |
| D. | 上述反应可能是2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O |
3.图为某化学反应的微观示意图,下列说法正确的是( )


| A. | 图中出现4种分子 | |
| B. | 参加反应的A2与B2两种物质的分子个数比为2:3 | |
| C. | 图中生成物有2种 | |
| D. | 图示反应前后原子个数不变 |
10.下列对物质的分类正确的是( )
| A. | 混合物:空气、石灰石、熟石灰 | B. | 合金:不锈钢、焊锡、铁矿石 | ||
| C. | 导体:石墨、汞、食盐水 | D. | 含氧化合物:氧气、水、氢氧化钾 |
4.2015年世界环境日的主题确定为:Think.Eat.Save.--思前、食后、厉行节约.下面做法符合这一主题的是( )
| A. | 生活中使用含磷洗衣粉能给水体提供养分,建议大量使用 | |
| B. | 大力开采矿物,保障金属材料的使用 | |
| C. | 采用焚烧的方法处理农作物秸秆和垃圾 | |
| D. | 推广利用太阳能、风能,缓解温室效应 |
5.如表是所列是两种元素的部分信息,请用化学用语将表格补充完整:
| 元素符号 | 离子结构示意图 | 离子符号 | 它们组成的单质相互反应的化学方程式 |
| Al | 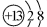 | Al3+ | 4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 |
| O |  | O2- |
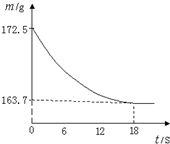 某纯碱样品只含有氯化钠杂质.为测定碳酸钠的质量分数,称取该样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.
某纯碱样品只含有氯化钠杂质.为测定碳酸钠的质量分数,称取该样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.