题目内容
(2010?达州)(1)利用如图所示装置可测定空气中氧气的含量.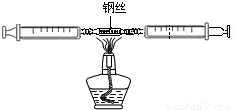
①实验现象,红色物质逐渐变成______.
②反应的化学方程式为______ 2CuO
【答案】分析:(1)在加热的条件下,铜丝与空气中的氧气反应生成黑色的氧化铜,停止加热冷却至室温,注射器内气体的体积大约减少了 ,由此可以得出:空气中氧气的体积分数大约为
,由此可以得出:空气中氧气的体积分数大约为 ;
;
(2)根据HCl+NaOH=NaCl+H2O的方程式,首先求出反应后所得溶液溶质NaCl的质量,再根据溶液溶质质量分数的计算公式求出反应后所得溶液溶质质量分数.
解答:解:(1)在加热热的条件下,铜丝与空气中的氧气反应生成黑色的氧化铜,反应的化学方程式为:2Cu+O2 2CuO;停止加热冷却至室温,注射器内气体的体积大约减少了
2CuO;停止加热冷却至室温,注射器内气体的体积大约减少了 ,由此可以得出:空气中氧气的体积分数大约为
,由此可以得出:空气中氧气的体积分数大约为 .
.
(2)设生成NaCl的质量为x
HCl+NaOH=NaCl+H2O
36.5 58.5
50g×7.3% x
 =
=
x= =5.85g
=5.85g
反应后所得溶液溶质质量分为 ×100%=5.85%
×100%=5.85%
故答为:(1)①黑色 ②2Cu+O2 2CuO ③约
2CuO ③约 ④空气中氧气的体积分数大约为
④空气中氧气的体积分数大约为
(2)反应后所得溶液溶质质量分数为5.85%
点评:本题主要考查了用铜丝测定空气里氧气含量的实验原理、操作步骤、实验现象、反应的化学方程式、实验结论等.由于装有铜丝的玻璃管和注射器的前端较细,为了使注射器里的空气中的氧气能充分的与铜丝反应,在试验过程中应来回交替推动注射器的活塞.
 ,由此可以得出:空气中氧气的体积分数大约为
,由此可以得出:空气中氧气的体积分数大约为 ;
;(2)根据HCl+NaOH=NaCl+H2O的方程式,首先求出反应后所得溶液溶质NaCl的质量,再根据溶液溶质质量分数的计算公式求出反应后所得溶液溶质质量分数.
解答:解:(1)在加热热的条件下,铜丝与空气中的氧气反应生成黑色的氧化铜,反应的化学方程式为:2Cu+O2
 2CuO;停止加热冷却至室温,注射器内气体的体积大约减少了
2CuO;停止加热冷却至室温,注射器内气体的体积大约减少了 ,由此可以得出:空气中氧气的体积分数大约为
,由此可以得出:空气中氧气的体积分数大约为 .
.(2)设生成NaCl的质量为x
HCl+NaOH=NaCl+H2O
36.5 58.5
50g×7.3% x
 =
=
x=
 =5.85g
=5.85g反应后所得溶液溶质质量分为
 ×100%=5.85%
×100%=5.85%故答为:(1)①黑色 ②2Cu+O2
 2CuO ③约
2CuO ③约 ④空气中氧气的体积分数大约为
④空气中氧气的体积分数大约为
(2)反应后所得溶液溶质质量分数为5.85%
点评:本题主要考查了用铜丝测定空气里氧气含量的实验原理、操作步骤、实验现象、反应的化学方程式、实验结论等.由于装有铜丝的玻璃管和注射器的前端较细,为了使注射器里的空气中的氧气能充分的与铜丝反应,在试验过程中应来回交替推动注射器的活塞.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目