题目内容
8.某无色混合气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的两种或几种,现将该混合气体依次通过下图所示装置,观察到:①A装置内未出现浑浊;②D装置内无水硫酸铜变蓝;最终收集到一定量干燥气体(假设每步反应都是完全的).
请回答下列问题:
(1)由①可知原混合气体中肯定不含二氧化碳;
(2)由②可知原混合气体中一定含有甲烷;
(3)原混合气体可能的组成有氮气.
分析 (1)根据二氧化碳气体和石灰水(氢氧化钙)反应生成碳酸钙沉淀可知原混合气体中肯定不含二氧化碳;
(2)甲烷燃烧生成水,无水硫酸铜遇水变蓝,据此答题;
(3)氮气的化学性质很稳定,常温下很难跟其他物质发生反应.
解答 解:(1)因为二氧化碳气体和石灰水(氢氧化钙)反应生成碳酸钙沉淀,而A装置内未见浑浊出现,说明原混合气体中肯定不含二氧化碳;
(2)因为甲烷燃烧生成水,无水硫酸铜遇水变蓝,故可判断原混合气体中一定含有甲烷;
(3)因为氮气的化学性质很稳定,常温下很难跟其他物质发生反应,所以原混合气体可能的组成有氮气.
故答案为:(1)二氧化碳;(2)甲烷;(3)氮气.
点评 此题主要是考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
2.除杂设计(括号内为杂质)所选试剂和操作都正确的是( )
| 序号 | 物质 | 选用试剂 | 操作 |
| A | CO2 (HCl) | NaOH溶液 | 洗气 |
| B | KC1O3 固体(KC1) | 加热至不再产生气体 | |
| C | KNO3 溶液(KOH) | CuSO4溶液 | 加入适量试剂,过滤、蒸发 |
| D | MgCl2 溶液(NaCl) | ①KOH溶液 ②稀盐酸 | 加入过量试剂①,过滤、洗涤 向所得固体中加入适量试剂②至固体恰好溶解 |
| A. | A | B. | B | C. | C | D. | D |
3.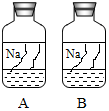 化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
【作出猜想】溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【限选试剂】酚酞试液、稀盐酸、石灰水、氯化钙溶液
【实施方案】
【实验反思】同学们经过分析,认为A溶液还可能是变质的NaOH溶液,请你利用上述试剂设计鉴定实验方案,完成实验报告.
 化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:
化学兴趣小组同学发现实验台上有两瓶标签破损的试剂瓶.小组同学针对这两瓶试剂展开研究:【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
【作出猜想】溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【限选试剂】酚酞试液、稀盐酸、石灰水、氯化钙溶液
【实施方案】
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 分别取少量待测液于试管中,向其中滴入酚酞试液 | 溶液变成红色 | 不可能是氯化钠溶液 |
| 实验二 | 另取少量待测液于试管中,向其中各滴入澄清石灰水 | 产生白色沉淀 | 可能是Na2SO3溶液和Na2CO3溶液中的一种,写出其中一个反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 或Na2SO3+Ca(OH)2=CaSO3↓+2NaOH |
| 实验三 | 另取少量待测液于试管中,分别加入足量的稀盐酸. | 若有无色无味的气体产生 | A是Na2CO3溶液 |
| 若有刺激性气味的气体产生 | B是Na2SO3溶液 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量A溶液于试管中,加入足量CaCl2溶液,再向上层清液中滴加无色酚酞溶液 | 产生白色沉淀,且溶液变成红色 | A溶液是部分变质的NaOH溶液 |
20.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
(1)乙物质可能是催化剂
(2)反应生成的甲物质的质量是7g
(3)该反应是分解反应
(4)测得反应后丁物质的质量为12g.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 3 | 5 | 20 | 7 |
| 反应后质量/g | 10 | 5 | 8 | 待测 |
(2)反应生成的甲物质的质量是7g
(3)该反应是分解反应
(4)测得反应后丁物质的质量为12g.
17.新华社2017年5月18日电,我国在南海海域成功连续8天稳定开采可燃冰(主要含甲烷水合物).与煤、石油相比,可燃冰污染小、热量大,而且全球储量足够人类使用1000年.某化学兴趣小组对海洋资源产生浓厚的兴趣.于是他们查阅资料,得到下列信息:
(1)可燃冰埋藏于海底的沉积物和陆地冻土的岩石中;
(2)可燃冰开采难度大,如果气化后的甲烷逸散到空气中,将会加剧全球气候变暖;
(3)海水“晒盐”得到的盐叫粗盐,含有CaCl2、Na2SO4等杂质.
他们分成两组对此进行探究:
Ⅰ组同学研究海底资源中的可燃冰,明确了两个问题:
(1)可燃冰在海底不燃烧的原因是没有与氧气接触,温度没有达到可燃冰的着火点;
(2)可燃冰形成的条件与温度、压强有关.
Ⅱ组同学研究海水物质资源中的主要化学成分,做了两个实验:
(1)模拟海水“晒盐”实验:将海水滴在玻璃片上,然后用吹风机吹干,产生白色固体,得到盐,这种结晶方法的原理是蒸发结晶.
(2)模拟粗盐除杂实验:
【提出问题】如何将粗盐中的CaCl2、Na2SO4杂质除掉
【可选试剂】稀H2SO4、稀HCl、NaOH溶液、BaCl2溶液、Na2CO3溶液
【进行实验】
【反思与评价】浩瀚的海洋将为我们全人类贡献丰富的资源.
同学们:除了可燃冰、食盐以外,你还能从化学学科角度再说出一种你所知道的海洋 资源吗?氯化镁.
(1)可燃冰埋藏于海底的沉积物和陆地冻土的岩石中;
(2)可燃冰开采难度大,如果气化后的甲烷逸散到空气中,将会加剧全球气候变暖;
(3)海水“晒盐”得到的盐叫粗盐,含有CaCl2、Na2SO4等杂质.
他们分成两组对此进行探究:
Ⅰ组同学研究海底资源中的可燃冰,明确了两个问题:
(1)可燃冰在海底不燃烧的原因是没有与氧气接触,温度没有达到可燃冰的着火点;
(2)可燃冰形成的条件与温度、压强有关.
Ⅱ组同学研究海水物质资源中的主要化学成分,做了两个实验:
(1)模拟海水“晒盐”实验:将海水滴在玻璃片上,然后用吹风机吹干,产生白色固体,得到盐,这种结晶方法的原理是蒸发结晶.
(2)模拟粗盐除杂实验:
【提出问题】如何将粗盐中的CaCl2、Na2SO4杂质除掉
【可选试剂】稀H2SO4、稀HCl、NaOH溶液、BaCl2溶液、Na2CO3溶液
【进行实验】
| 步骤 | 过程 | 现象 | 实验解析 |
| 第一步 |  | 产生白色沉淀 | 加入过量溶液Na2CO3的目的是除去氯化钙和过量的氯化钡 |
| 第二步 |  | 有气泡产生 | 化学反应方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| 第三步 | 蒸发所得溶液 | 析出白色固体 | 得到较纯净的食盐 |
同学们:除了可燃冰、食盐以外,你还能从化学学科角度再说出一种你所知道的海洋 资源吗?氯化镁.
18.大气中二氧化碳含量剧增,引起的环境问题是( )
| A. | 酸雨 | B. | 温室效应 | C. | 臭氧层破坏 | D. | 白色污染 |

