题目内容
3.将NaCl与NaNO3的混合物1.47g完全溶于4.8g水中,加入12.2gAgNO3溶液,恰好完全反应,所得溶液质量比反应前少2.87g,求所得溶液中溶质的质量分数?(保留1%)分析 由题意可知,溶液减少的质量即为氯化银沉淀的质量,利用化学方程式中已知氯化银的量可求硝酸钠的质量,再利用溶质质量分数的计算求出滤液的溶质质量分数.
解答 解:由题意可知,溶液减少的质量即为氯化银沉淀的质量,所以硝酸银的质量为 2.87g;
设固体混合物中氯化钠的质量为x,反应后生成硝酸钠的质量为y.
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5 85
x 2.87g y
$\frac{58.5}{x}=\frac{143.5}{2.87g}=\frac{85}{y}$
x=1.17g
y=1.7g
反应后滤液中溶质的质量分数为$\frac{1.7g+(1.47g-1.17g)}{1.47g+4.8g+12.2g-2.87g}×$100%≈13%
点评 本题主要考查有关化学方程式的计算和溶质质量分数的计算,属常规性化学方程式的计算题.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.下列微粒观点的说法正确的是( )
| A. | 水和酒精混合时体积变小,说明分子不断运动 | |
| B. | 物质都是由分子构成的 | |
| C. | 蔗糖水不导电,说明蔗糖分子不运动 | |
| D. | 氢气和液氢都可以作燃料,说明相同分子的物质其化学性质相同 |
15.化学学习中,我们可以发现或总结具有一定规律性的知识,下列描述中,正确的是( )
| A. | 酸溶液能使紫色石蕊试液变红色,则能使紫色石蕊试液变红的溶液一定显酸性 | |
| B. | 催化剂一定能加快化学反应速率 | |
| C. | 盐中都一定含有金属元素 | |
| D. | 复分解反应中有沉淀、气体或水生成,则有上述物质产生的反应一定是复分解反应 |
12.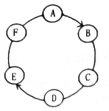 A、B、C、D、F均为初中化学中不同类别的物质,它们的变化关系如图所示,其中红棕色物质A在一定条件下可以转化为单质B,C、D常用来配制农药波尔多液.“-”表示相连的两种物质能发生反应,“→”表示物质转化的方向.下列有关说法不正确的是( )
A、B、C、D、F均为初中化学中不同类别的物质,它们的变化关系如图所示,其中红棕色物质A在一定条件下可以转化为单质B,C、D常用来配制农药波尔多液.“-”表示相连的两种物质能发生反应,“→”表示物质转化的方向.下列有关说法不正确的是( )
 A、B、C、D、F均为初中化学中不同类别的物质,它们的变化关系如图所示,其中红棕色物质A在一定条件下可以转化为单质B,C、D常用来配制农药波尔多液.“-”表示相连的两种物质能发生反应,“→”表示物质转化的方向.下列有关说法不正确的是( )
A、B、C、D、F均为初中化学中不同类别的物质,它们的变化关系如图所示,其中红棕色物质A在一定条件下可以转化为单质B,C、D常用来配制农药波尔多液.“-”表示相连的两种物质能发生反应,“→”表示物质转化的方向.下列有关说法不正确的是( )| A. | 做反应A→B的实验,要先通入一种气体再加热A | |
| B. | 反应B+C→是湿法冶炼金属的先驱 | |
| C. | D→E只能发生复分解反应 | |
| D. | A与F反应后的溶液为黄色 |
13.下列对水的叙述正确的是( )
| A. | 水的三态变化,能实现水的自身净化和水资源的重新分配 | |
| B. | 水的三态变化,是由于水分子的体积改变 | |
| C. | 过滤和吸附能除去水中所有的杂质 | |
| D. | 水是由氢气和氧气组成 |
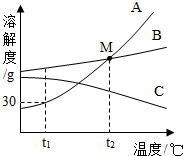 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: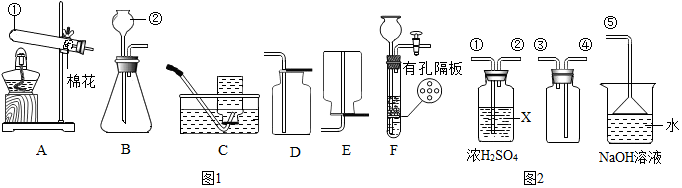
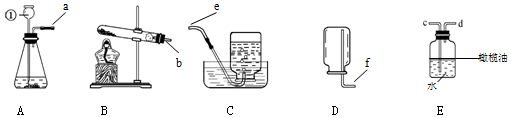
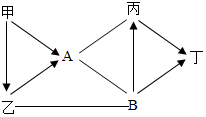 如图中都是初中化学常见物质,其中A、B为单质,B为黑色固体,甲、乙、丙、丁是化合物,甲和乙组成元素相同且通常为液态,丙和丁组成元素相同且通常为气态.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物或生成物已略去.
如图中都是初中化学常见物质,其中A、B为单质,B为黑色固体,甲、乙、丙、丁是化合物,甲和乙组成元素相同且通常为液态,丙和丁组成元素相同且通常为气态.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物或生成物已略去.