题目内容
12.下列有关说法正确的组合为( )①可以用肥皂水区别软水和硬水;
②为了保护水资源,应禁止使用化肥和农药;
③可以用带火星的木条区别空气和氧气;
④呼出气体中含量最多的气体是二氧化碳;
⑤稀有气体可以用作电光源;
⑥可燃性气体点燃之前,应该检验气体的纯度.
| A. | ①②④⑥ | B. | ①③④⑥ | C. | ①③⑤⑥ | D. | ③④⑤⑥ |
分析 ①肥皂水能够区别软水和硬水;
②化肥和农药可合理使用;
③根据氧气支持燃烧分析;
④呼出气体中含量最多是氮气;
⑤稀有气体可以用作电光源;
⑥可燃性气体点燃之前,应该检验气体的纯度.
解答 解:①加肥皂水后生成泡沫多的是软水,生成泡沫少的是软水,所以可以用肥皂水区别软水和硬水,故正确;
②为了保护水资源,应合理使用化肥和农药,不是禁止,故错误;
③氧气支持燃烧,可以用带火星的木条区别空气和氧气,故正确;
④呼出气体中含量最多的气体是氮气,故错误;
⑤稀有气体用于电光源是利用稀有气体通电后发生不同颜色的光,可以用作电光源,故正确;
⑥为防止爆炸,可燃性气体点燃之前,应该检验气体的纯度,故正确.
故选C.
点评 本题考查的知识点较多,但难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
3.空气中含量较多,可用作食品包装以防腐的保护气的是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
20.空气中氧气含量测定的再认识.
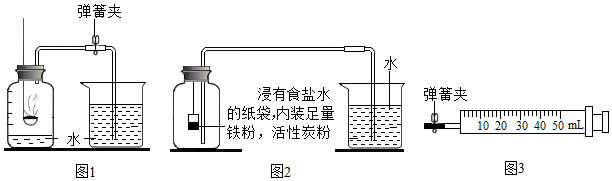
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
步骤如下:
①用弹簧夹夹紧橡皮管.
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子.
③待装置冷却后打开弹簧夹.
④观察并记录水面的变化情况.
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5.
【实验改进1】
Ⅰ.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图2实验装置,再次测定空气中氧气含量.装置中的食盐水和活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%.(消耗的水的体积忽略不计,计算结果保留一位小数).
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想(Ⅱ)(填序号)一定是错误的,理由是化学反应前后元素种类不变.
实验改进2】
使用图3装置进行实验.实验前应先进行的操作
是检查装置的气密性.
【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
数据处理】实验中需要记录的数据是注射器中原来的空气体积,反应后剩余气体的体积.
计算得出氧气约占空气总体积的$\frac{1}{5}$.
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等.(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
步骤如下:
①用弹簧夹夹紧橡皮管.
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子.
③待装置冷却后打开弹簧夹.
④观察并记录水面的变化情况.
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5.
【实验改进1】
Ⅰ.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图2实验装置,再次测定空气中氧气含量.装置中的食盐水和活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%.(消耗的水的体积忽略不计,计算结果保留一位小数).
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想(Ⅱ)(填序号)一定是错误的,理由是化学反应前后元素种类不变.
实验改进2】
使用图3装置进行实验.实验前应先进行的操作
是检查装置的气密性.
【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
数据处理】实验中需要记录的数据是注射器中原来的空气体积,反应后剩余气体的体积.
计算得出氧气约占空气总体积的$\frac{1}{5}$.
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等.(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.

7. 图为电解水实验示意图,下列有关说法中正确的是( )
图为电解水实验示意图,下列有关说法中正确的是( )
 图为电解水实验示意图,下列有关说法中正确的是( )
图为电解水实验示意图,下列有关说法中正确的是( )| A. | 与直流电源正极相连的玻璃管内产生的气体可以燃烧 | |
| B. | 该实验可以得出结论,水是由氢气和氧气组成的 | |
| C. | 与直流电源的正极和负极相连管内产生气体的质量比为1:2 | |
| D. | a玻璃管连接直流电源的负极 |
17.下列说法正确的是( )
| A. | 木炭燃烧后生成红色固体 | |
| B. | 镁条在空气中燃烧发出耀眼的白光 | |
| C. | 红磷在空气中燃烧产生大量白雾 | |
| D. | 蜡烛燃烧既是氧化反应也是化合反应 |
1.自来水是我国目前主要生活饮用水,如表是我国的饮用水水质标准的内容.
(1)自来水中的游离氯有少量可转变成氯离子,氯离子的符号是Cl-,自来水的主要成分是水,请你用化学符号表示:2个水分子2H2O.
(2)表格中的感官指标表现的是自来水的物理(填“物理”或“化学”)性质,自来水属于混合物(填“纯净物”或“混合物”).
(3)在下列净化水的操作中,可以降低水的硬度的是d.
a、吸附 b、沉淀 c、过滤 d、蒸馏
(4)在天然水净化过程中,人们常用活性炭去除异味和色素.这是利用活性炭的吸附作用.此外还需消毒杀菌,ClO2可用于消毒,ClO2中氯元素的化合价为+4价.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | 铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.01.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)表格中的感官指标表现的是自来水的物理(填“物理”或“化学”)性质,自来水属于混合物(填“纯净物”或“混合物”).
(3)在下列净化水的操作中,可以降低水的硬度的是d.
a、吸附 b、沉淀 c、过滤 d、蒸馏
(4)在天然水净化过程中,人们常用活性炭去除异味和色素.这是利用活性炭的吸附作用.此外还需消毒杀菌,ClO2可用于消毒,ClO2中氯元素的化合价为+4价.
2.关于CO2、O2、H2O2、MnO2四种物质,下列说法中正确的是( )
| A. | 都含有1个氧分子 | B. | 都含有2个氧原子 | C. | 都具有相同性质 | D. | 都含有氧元素 |