题目内容
10.硅酸钠(Na2SiO3)是我国优先发展的精细化工产品.现以125t石英砂(其中SiO2质量分数为96%)为原料,与足量的NaOH溶液恰好完全反应,得到硅酸钠溶液的质量为610t.已知:工业制备硅酸钠的反应为:2NaOH+SiO2═Na2SiO3+H2O试计算:
(1)125t石英砂中SiO2的质量.
(2)所得硅酸钠溶液中溶质的质量分数(石英砂中杂质不溶于水).
分析 (1)根据石英砂中SiO2质量分数为96%,由石英砂的质量计算其中SiO2的质量;
(2)根据反应的化学方程式,利用石英砂中SiO2的质量计算硅酸钠的质量,进一步计算硅酸钠溶液中溶质的质量分数.
解答 解:(1)石英砂中的SiO2的质量=125t×96%=120t;
(2)设所得Na2SiO3 的质量为x
2NaOH+SiO2═Na2SiO3+H2O
60 122
120t x
$\frac{60}{120t}$=$\frac{122}{x}$
x=244t
C%=$\frac{244t}{610t}$=40%
故答案为:(1)120t;
(1)所得硅酸钠溶液中溶质质量分数为40%.
点评 根据化学方程式进行计算时,所使用的物质的质量应为纯净物的质量,不可把混合物的质量直接代入进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.除去如表所示物质中的杂质(括号内为杂质),所选用试剂及操作均正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | Na2SO4(NaOH) | 稀硫酸 | 加过量的稀硫酸、蒸发结晶 |
| B | NaCl(Na2CO3) | BaCl2溶液 | 加入适量的BaCl2溶液,过滤,将滤渣洗涤、干燥 |
| C | KCl(K2CO3) | 稀盐酸 | 加过量的稀盐酸,蒸发结晶 |
| D | CaO(CaCO3) | 稀盐酸 | 加入足量的稀盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
1.下列化学方程式不符合题意的是( )
| A. | 自制简易灭火器原理:Na2CO3+2HCl═2NaCl+H2O+CO2↑ | |
| B. | 用生石灰处理硫酸厂废液:Ca(OH)2+H2SO4═CaSO4+2H2O | |
| C. | 不能用铁制容器盛装硫酸铜溶液的原因:Fe+CuSO4═FeSO4+Cu | |
| D. | 证明铁是金属活动性顺序表中氢之前的金属:Fe+2HCl═FeCl2+H2↑ |
18.下列物质不需要密封保存的是( )
| A. | 大理石 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氢氧化钠 |
5. 氯化铵(NH4Cl)是一种重要的化工原料.
氯化铵(NH4Cl)是一种重要的化工原料.
(1)氯化铵可用作氮肥.
(2)氯化铵的溶解度如下表所示:
20℃时,向盛有37.2g NH4Cl的烧杯中,加入100g的水,充分溶解后形成溶液的是饱和溶液(填“饱和”或“不饱和”).
(3)如图所示,小烧杯中盛放的是(2)中所得的溶液.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.氢氧化钠 C.硝酸铵 D.氧化钙.
 氯化铵(NH4Cl)是一种重要的化工原料.
氯化铵(NH4Cl)是一种重要的化工原料.(1)氯化铵可用作氮肥.
(2)氯化铵的溶解度如下表所示:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
(3)如图所示,小烧杯中盛放的是(2)中所得的溶液.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.氢氧化钠 C.硝酸铵 D.氧化钙.
15.下列物质中,能与水反应且放热的是( )
| A. | 碳酸钙 | B. | 生石灰 | C. | 氢氧化钠 | D. | 食盐 |


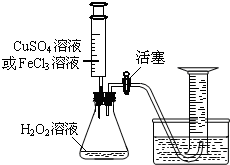 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究: