题目内容
19.12g碳单质完全燃烧放出的热量为E1,碳不完全燃烧生成一氧化碳放出的热量为E2,则56g一氧化碳完全燃烧放出的热量为2E1-2E2..分析 根据一氧化碳的质量求出碳单质的质量,再根据碳单质完全燃烧放出的热量和碳不完全燃烧生成一氧化碳放出的热量分析计算.
解答 解:设生成56g一氧化碳的需要碳的质量为x
2C+O2$\frac{\underline{\;点燃\;}}{\;}$ 2CO
24 56
x 56g
$\frac{24}{56}=\frac{x}{56g}$ 解得:x=24g
56g一氧化碳完全燃烧放出的热量为:$\frac{24g}{12g}×$E1-$\frac{24g}{12g}$×E2=2E1-2E2.
故答为:2E1-2E2.
点评 本题的难度不大,掌握碳与氧气完全燃烧生成了二氧化碳,不完全燃烧生成了一氧化碳,一氧化碳燃烧生成了二氧化碳是解答本题的基础.

练习册系列答案
相关题目
10.下列实验中,可验证物质的化学性质的是( )
| A. |  金属刻划 | B. |  闻气味 | C. | 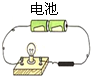 石墨导电 | D. |  鲜花变色 |
11.从分子的角度解释“湿衣服晾干”,下列说法错误的是( )
| A. | 水分子在不断运动 | B. | 水分子之间的间隔变大 | ||
| C. | 水分子本身不发生变化 | D. | 水分子的体积变大 |
9.下列实验的基本操作正确的是( )
| A. | 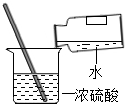 浓硫酸的稀释 | B. | 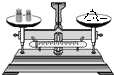 称量一定质量的食盐 | ||
| C. | 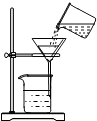 过滤 | D. | 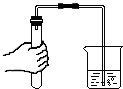 检查装置的气密性 |
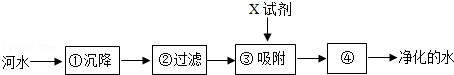
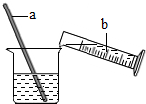 实验室中常需要使用硫酸.
实验室中常需要使用硫酸.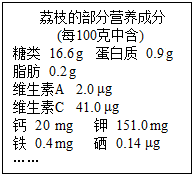 又到六月荔枝成熟的季节,九年级的几个同学结伴到彬彬家去摘荔枝和进行野炊活动.
又到六月荔枝成熟的季节,九年级的几个同学结伴到彬彬家去摘荔枝和进行野炊活动.