题目内容
通常情况下是一种气体,它的一个分子由两个原子构成,一切生命活动离不开它,火苗遇到它窜的高……。它是 ( )
A.二氧化碳 B.氮气 C.氧气 D.水蒸气
C

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案20.
21.
22.
23.
24.
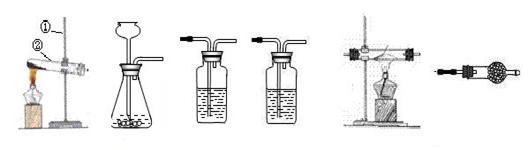
下图是提纯CO、CO2混合气体中的CO并还原氧化铁的示意图。请回答有关问题:

(1) 为避免CO污染空气,并回收利用CO,方框中连接的是D和E,导管接口的连接顺序为a→___
→___→____。D装置中NaOH的作用是________________________________。如果导管连接错误,后果是_____________________________________。
(2) 实验进行一段时间后,B装置的玻璃管中的现象为_______________ _________,反应的化学方程式为________________ ____________。用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是 。
____________。用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是 。
(3) 实验结束后,要从A装置的混合溶液中回收得到较纯净的NaOH固体。
资料显示,在不同温度下NaOH的溶解度如下:
| 温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/(g/100 g水) | 64 | 85 | 138 | 203 | 285 | 376 |
利用实验室的试剂和条件,实验步骤如下(其中Ⅰ、Ⅱ、Ⅲ为实验操作):

请回答下列 问题:
问题:
① 化学式:A.___________;
② 操作名称:Ⅲ. ________________________;
________________________;
③ 如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是
。
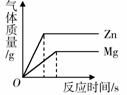
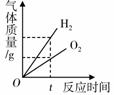
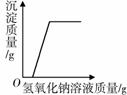
下列叙述与对应的坐标图表示正确的是( )
|
|
|
|
|
| A.向硝酸钾的饱和溶 液中加入氯化钠 | B.将相同质量的Zn粉 和Mg粉分别加入 足量的稀盐酸中 | C.水的电解 | D.向盐酸和氯化铁混合 溶液中加入过量的氢 氧化钠溶液 |
废铁屑的主要成分是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示:

在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe====3FeSO4外还有
(只需写一条化学方程式)。
滤液M中肯定含有的溶质的化学式是 。
在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和 。
滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | ||||||||
根据溶解度表,硫酸亚铁晶体(FeSO4·7H2O)冷却结晶温度最高不 超过 ℃。
超过 ℃。
在化学反应中,将有元素化合价变化的反应定义为氧化还原反应。下列反应类型肯定是氧化还原反应的是 (选填字母序号)。
| A.化合反应 | B.置换反应 | C.分解反应 | D.复分解反应 |
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等。
将无水硫酸亚铁(FeSO4)隔绝空气加强热,分解产物有氧化铁和另两种氧化物,试写出该反应的化学方程式: 。
 ,乙同学认为自己是正确的。B中的反应方程式是 。D中的现象是 。
,乙同学认为自己是正确的。B中的反应方程式是 。D中的现象是 。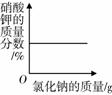
 泼,是可燃物
泼,是可燃物 酸钾 双氧水
酸钾 双氧水 