题目内容
6.在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如下所示.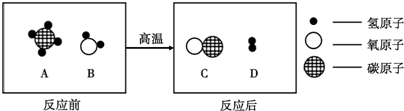
(1)一个A分子中共含有5个原子,B代表的是H2O(填化学式).
(2)四种物质中,属于单质的是D(填图中的字母,下同),可用作燃料的是ACD.
(3)在该反应中,以下叙述正确的是bd.
a.属于置换反应 b.原子种类没有改变
c.分子的个数没有改变 d.A物质中某元素的质量分数为25%
(4)在该反应中,生成C和D的质量比为14:3.
分析 将图示以及符号意义转化为更直观的化学反应,从而结合反应进行方程式的进行分析与判断.从图示可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2,据此分析解决即可.
解答 解:由化学反应的微观示意图图示可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2,由此可知:
(1)A是CH4,一个分子中共含有5个原子,B代表的是水,化学式是:H2O.
(2)在CH4、H2O、CO、H2四种物质中,属于单质的是H2,能用作燃料的是CH4、CO、H2.
(3)a.该反应是的反应物是两种化合物,不属于置换反应.故a叙述不正确;
b.对比反应前后微粒的变化可知,原子种类没有改变.故b叙述正确;
c.对比反应前后微粒的变化可知,分子的个数发生了改变.故c叙述不正确.
d、A物质是甲烷,氢元素的质量分数为$\frac{1×4}{12+1×4}×100%$=25%,故d叙述正确.
(4)在该反应中,生成C和D的质量比为:28:(3×2)=14:3.
故答为:(1)5,H2O;(2)D,H2O;(3)bd;(4)14:3.
点评 解决本类问题的方法是分清分子中由何种原子构成,每种原子有几个,写出化学式和反应的方程式,再对有关的问题进行分析解答.

练习册系列答案
相关题目
17.某化合物在一定量的氧气中充分燃烧后,经测定,产物中只有二氧化碳和水,下列关于该化合物的说法正确的是( )
| A. | 一定含碳氢氧三种元素 | B. | 只含有碳和氢两种元素 | ||
| C. | 一定含碳和氢元素,可能含氧元素 | D. | 无法确定 |
14.下列药品①苛性钠②碳酸钠晶体③浓盐酸④浓硫酸,未经密封保存,经过一段时间后,质量增加的是( )
| A. | ①和② | B. | ②和③ | C. | ①和④ | D. | ③和④ |
1.下列说法不正确的是( )
| A. | 碱分子里氢氧根的数目与金属离子在该碱中的化合价数相等 | |
| B. | 能电离出氢氧根离子的化合物一定是碱 | |
| C. | 由金属离子和酸根离子组成的化合物叫做盐 | |
| D. | KHSO4能电离出H+,但它不是酸,而是盐 |
11.环境污染已对人类造成重大威胁.下列名词与环境污染无关的是( )
| A. | 潮汐 | B. | 酸雨 | C. | 空气污染指数 | D. | 工业废水 |
18.空气是一种宝贵的自然资源,从分离空气的成分中不能得到的气体是( )
| A. | 用作医疗急救的氧气 | B. | 用作霓虹灯中填充的稀有气体 | ||
| C. | 用作清洁燃料的氢气 | D. | 用作食品防腐剂的氮气 |
15.在溶液中,溶质的存在形式为( )
| A. | 小颗粒 | B. | 小液滴 | C. | 单个分子或离子 | D. | 三种情况都有 |
