题目内容
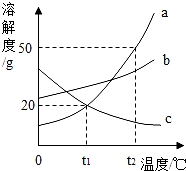
如图是三种固体物质的溶解度曲线.
(1)物质c的溶解度随温度的升高而 ;
(2)物质a的溶解度大于物质c的溶解度的温度范围是 ;
(3)t2℃时,用50g水配制物质a的饱和溶液,至少需要 g a物质;
(4)t1℃时,a和c的饱和溶液的溶质质量分数都是 ;
(5)将t2℃时a、b、c三种物质的饱和溶液降温至t1℃(溶剂量不变),溶液中溶质质量分数不变的是 .
【考点】固体溶解度曲线及其作用;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】(1)据溶解度曲线可知物质的溶解度随温度变化情况;
(2)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(3)据该温度下a的溶解度分析解答;
(4)据饱和溶液中溶质的质量分数解答;
(5)据物质的溶解度随温度变化情况及溶质的质量分数计算方法解答.
【解答】解:(1)由图可知:物质c的溶解度随温度的升高而 减小;
(2)由图可知:温度大于>t1℃物质a的溶解度大于物质c的溶解度;
(3)t2℃时a的溶解度是50g,即100g水中最多溶解50g的a,所以用50g水配制物质a的饱和溶液,至少需要 25g a物质;
(4)饱和时质量分数= ×100%,a和c的溶解度相等,都是20g,所以t1℃时,a和c的饱和溶液的溶质质量分数都是
×100%,a和c的溶解度相等,都是20g,所以t1℃时,a和c的饱和溶液的溶质质量分数都是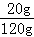 ×100%≈16.7%;
×100%≈16.7%;
(5)将t2℃时a、b、c三种物质的饱和溶液降温至t1℃(溶剂量不变),c的溶解度随温度降低而增大,无溶质析出,溶液中溶质、溶剂的质量不变,溶质质量分数不变,ac溶解度随温度降低而减小,均析出溶质,溶质的质量分数要减小;
故答案为:(1)减小; (2)>t1℃; (3)25; (4)16.7%; (5)c.
【点评】了解溶解度概念的含义、溶质的质量分数计算、溶解度曲线的意义等知识,较好考查了学生分析、解决问题的能力.

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案


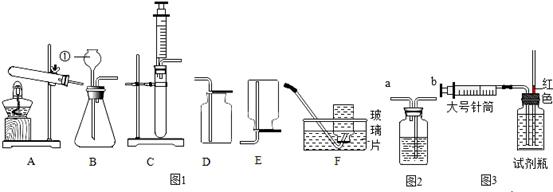
 试剂瓶中加 入200mL水(恰好加满),塞紧双孔橡皮塞;
试剂瓶中加 入200mL水(恰好加满),塞紧双孔橡皮塞; ,体操运动员在上器械之前常在手上搓一种白色粉末,其中含有碳酸镁、氧化镁等物质.这种白色粉末属于( )
,体操运动员在上器械之前常在手上搓一种白色粉末,其中含有碳酸镁、氧化镁等物质.这种白色粉末属于( )
 瓶中水的体积不到总容积的
瓶中水的体积不到总容积的 ,你认为其原因可能是 、 .(写2点)
,你认为其原因可能是 、 .(写2点)