题目内容
请结合图中所示实验装置回答有关问题:
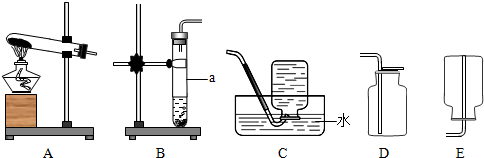
(1)写出装置中标号仪器的名称.a
(2)在实验室可以选择A、D装置可以制取氧气,写出利用以上装置实验室制取氧气的化学方程式
(3)你所组装的上述制取氧气的装置
分析:A装置要求反应物是固体,反应条件是加热;D装置收集的气体密度需大于空气;
解答:解:(1)仪器名称为酒精灯;试管
(2)A装置要求反应物是固体,反应条件是加热,实验室制氧气适合此条件的有高锰酸钾制氧气和氯酸钾和二氧锰混合物制氧气,两种方法的区别在于高锰酸钾制氧气需在试管口放一团棉花.因此利用此装置只能是氯酸钾制氧气.故化学方程式为2KClO3
2KCl+3O2↑;
(3)实验室制取二氧化碳用的是大理石和稀盐酸,大理石是固体,稀盐酸是液体,反应条件是常温,故应选用固体常温型装置,选B.
故答案为:(1)酒精灯;试管(2)2KClO3
2KCl+3O2↑;(3)反应物的状态不同,反应条件不同;
(2)A装置要求反应物是固体,反应条件是加热,实验室制氧气适合此条件的有高锰酸钾制氧气和氯酸钾和二氧锰混合物制氧气,两种方法的区别在于高锰酸钾制氧气需在试管口放一团棉花.因此利用此装置只能是氯酸钾制氧气.故化学方程式为2KClO3
| ||
(3)实验室制取二氧化碳用的是大理石和稀盐酸,大理石是固体,稀盐酸是液体,反应条件是常温,故应选用固体常温型装置,选B.
故答案为:(1)酒精灯;试管(2)2KClO3
| ||
点评:实验室制取气体发生装置根据反应物状态和反应条件来选择,收集装置根据气体的密度和溶解性来选择.

练习册系列答案
相关题目
为测定H2SO4和CuSO4的混合溶液中溶质的含量,小强和小国设计并进行了以下实验.
【查阅资料】①Cu(OH)2固体受热易分解产生CuO和H2O;②BaSO4固体受热难分解.
【实验一】目的:测定100.0g混合溶液中CuSO4的质量
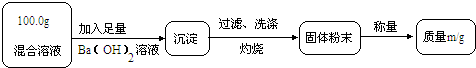
(1)小强认为m1是CuO的质量,小国提出质疑,认为m1是 的质量.
(2)为得到CuO的质量,小国决定将Ba(OH)2溶液换成另一种溶液,该溶液可以是 (填字母).
A.NaOH溶液、B.KOH溶液、C.BaCl2溶液
(3)改进实验后小国得到8.0g CuO,试求100.0g混合溶液中CuSO4的质量.
解:
【实验二】目的:测定100.0 g混合溶液中H2SO4的质量分数
主要实验步骤如下: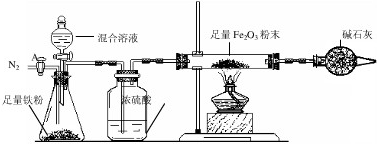
a.按图组装仪器,检查气密性,装好药品,其中Fe2O3的质量为m2g;
b.打开活塞A,通入N2一段时间,关闭活塞A;
c.点燃酒精灯,逐滴加入100.0g混合溶液;
d.测定反应过程中硬质玻璃管内物质的质量(见表格所示);
e.待反应结束后,熄灭酒精灯,打开活塞A,缓缓通一会儿N2.
记录数据
过滤、洗涤干燥、称量
(4)请结合以上实验数据(假设与Fe2O3反应的气体的损耗忽略),计算100.0g混合溶液中H2SO4的质量分数为 .(可能用到的相对分子质量:Fe2O3-160,H2SO4-98)
【查阅资料】①Cu(OH)2固体受热易分解产生CuO和H2O;②BaSO4固体受热难分解.
【实验一】目的:测定100.0g混合溶液中CuSO4的质量

(1)小强认为m1是CuO的质量,小国提出质疑,认为m1是
(2)为得到CuO的质量,小国决定将Ba(OH)2溶液换成另一种溶液,该溶液可以是
A.NaOH溶液、B.KOH溶液、C.BaCl2溶液
(3)改进实验后小国得到8.0g CuO,试求100.0g混合溶液中CuSO4的质量.
解:
【实验二】目的:测定100.0 g混合溶液中H2SO4的质量分数
主要实验步骤如下:

a.按图组装仪器,检查气密性,装好药品,其中Fe2O3的质量为m2g;
b.打开活塞A,通入N2一段时间,关闭活塞A;
c.点燃酒精灯,逐滴加入100.0g混合溶液;
d.测定反应过程中硬质玻璃管内物质的质量(见表格所示);
e.待反应结束后,熄灭酒精灯,打开活塞A,缓缓通一会儿N2.
记录数据
| 时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
| 质量/g | m2 | m2-1.6 | m2-3.0 | m2-4.0 | m2-4.8 | m2-4.8 |
(4)请结合以上实验数据(假设与Fe2O3反应的气体的损耗忽略),计算100.0g混合溶液中H2SO4的质量分数为



 2H2O+O2↑
2H2O+O2↑