题目内容
化学兴趣小组在进行盐酸和氧氧化钠溶液中和反应实验时,发现它们混合后没有明显现象.用什么方法证明它们已经发生了反应呢?小组的陈东和张丽进行如下探究.
(1)陈东:我用pH试纸监测.
实验过程如下:①用pH试纸测定NaOH溶液的pH,②将足量盐酸加入氧氧化钠溶液中.③用pH试纸测定混合后溶液的pH;如果______.说明它们已经发生了反应.
(2)张丽:我用酸碱指示剂监测.
实验过程如下:______;如果______.说明它们已经发生了反应.
(3)除了上述方法外.我还可以用以下方法证明它们已经发生了反应(填写实验方案):______.说明它们已经发生了反应.
(1)陈东:我用pH试纸监测.
实验过程如下:①用pH试纸测定NaOH溶液的pH,②将足量盐酸加入氧氧化钠溶液中.③用pH试纸测定混合后溶液的pH;如果______.说明它们已经发生了反应.
(2)张丽:我用酸碱指示剂监测.
实验过程如下:______;如果______.说明它们已经发生了反应.
(3)除了上述方法外.我还可以用以下方法证明它们已经发生了反应(填写实验方案):______.说明它们已经发生了反应.
(1)氢氧化钠溶液呈碱性,其pH值大于7,若反应则会由于氢氧化钠的减少而使溶液的pH值减小,故如果反应,则溶液的pH值会减小;
(2)根据酚酞遇碱变红,遇酸或中性溶液不变色的性质,可以选择酚酞试液来检测,故可以向滴有酚酞的氢氧化钠溶液中加入足量的稀盐酸,若观察到红色消失则可以证明它们发生了反应;
(3)由于酸可以和活泼金属反应生成氢气,而氢氧化钠溶液不能和金属反应,所以可以选择铁粉来检验它们是否反应;
故答案为:(1)pH由大变小;
(2)①在NaOH溶液中加入几滴酚酞试液,②将足量盐酸加入氢氧化钠溶液中;溶液由红色变为无色;
(3)①向一支装有盐酸的试管加入足量氢氧化钠溶液,②向试管中加入少量铁粉(其他活泼金属粉末或碳酸钠等碳酸盐);如果没有气泡产生.
说明:此题为开放性试题,只要溶液混合前后现象有明显差别或其他合理答案均给分,但用指示剂的方法不给分.
(2)根据酚酞遇碱变红,遇酸或中性溶液不变色的性质,可以选择酚酞试液来检测,故可以向滴有酚酞的氢氧化钠溶液中加入足量的稀盐酸,若观察到红色消失则可以证明它们发生了反应;
(3)由于酸可以和活泼金属反应生成氢气,而氢氧化钠溶液不能和金属反应,所以可以选择铁粉来检验它们是否反应;
故答案为:(1)pH由大变小;
(2)①在NaOH溶液中加入几滴酚酞试液,②将足量盐酸加入氢氧化钠溶液中;溶液由红色变为无色;
(3)①向一支装有盐酸的试管加入足量氢氧化钠溶液,②向试管中加入少量铁粉(其他活泼金属粉末或碳酸钠等碳酸盐);如果没有气泡产生.
说明:此题为开放性试题,只要溶液混合前后现象有明显差别或其他合理答案均给分,但用指示剂的方法不给分.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
 化学兴趣小组在学习了酸、碱、盐的化学性质后,进行了如图所示的实验:
化学兴趣小组在学习了酸、碱、盐的化学性质后,进行了如图所示的实验:
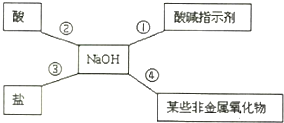 某化学兴趣小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学兴趣小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题: