题目内容
完成下列研究性学习的有关内容;探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
[研究方案]先称取一定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止.根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量.(学习小组同学事先查阅资料获知,二氧化锰的质量在反应前后不变且在水中难溶)
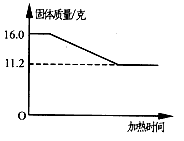
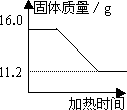
[解决问题]实验测得固体混合物质量随加热时间变化的相关数据如下图所示.请你完成下表:
[继续研究]为了分离回收二氧化锰和氯化钾,他们在反应后的固体混合物中加入80g水使其中的氯化钾完全溶解,然后通过过滤二氧化锰与液体分离.请你计算他们得到的滤液中氯化钾的质量分数.(过滤中水的损失不计).
答案:
解析:
解析:
|
(1)
(2)略解:设:混合物中KClO3的质量为x;生成的KCl质量为y 则m O2=16.0 g-11.2 g=4.8 g 2KClO3 245 149 96 X y 4.8 得x=12.25 g y=7.45 g ∴KClO3的质量分数= ∴KCl的质量分数= |

练习册系列答案
相关题目
 完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
[研究方案]先称取-定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止.根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量.(学习小组同学事先查阅资料获知,氯酸钾分解的化学方程式为:2KClO3 2KCI+3O2↑ 二氧化锰的质量在反应前后不变且在水中难溶.)
2KCI+3O2↑ 二氧化锰的质量在反应前后不变且在水中难溶.)
[解决问题]实验测得固体混合物质量随加热时间变化的相关数据如图所示.请你完成下表:
[继续研究]为了分离回收二氧化锰和氯化钾,他们在反应后
| 反应中产生氧气的质量/克 | 原混合物中氯酸钾的质量/克 | 原混合物中氯酸钾的质量分数 |

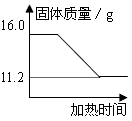
(2)[继续研究]为了分离回收二氧化锰和氯化钾,他们在反应后的固体混合物中加入80g水使其中的氯化钾完全溶解,然后通过过滤二氧化锰与液体分离。请你计算他们得到的滤液中氯化钾的质量分数。(过滤中水的损失不计)。

 完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.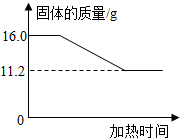 (2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
(2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.