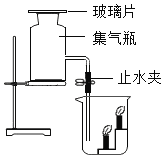
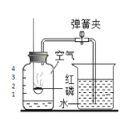
题目内容
【题目】图是常见物质之间的相互反应关系,其中甲、乙、丙、丁都是固体,且甲、乙、丙呈黑色,丁呈红色; A和B常温时呈液态,且含有相同的元素组成.请你推断:
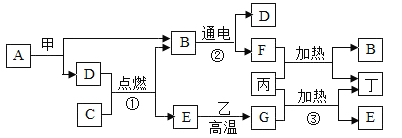
(1)下列物质的化学式:甲:_____;乙:_____;丙:_____;
(2)写出图中①②③反应的化学方程式:①_____;②_____,该反应的基本类型_____;③_____。
【答案】MnO2 C CuO  或
或
 分解反应
分解反应 ![]()
【解析】
B在常温时为液态,且在通电条件下能生成D和F,说明B为水,A为液态,具有和B相同的元素组成,所以A为过氧化氢,故可以推出在A中加入的黑色固体甲为二氧化锰;过氧化氢分解生成的D为氧气,水通电生成的F为氢气,F和丙在加热的条件下能生成B和红色固体丁,即H2+丙→H2O+丁,说明此反应利用的是氢气的还原性,发生的是置换反应,所以生成的红色固体丁为铜,黑色固体丙为氧化铜;丙与G在加热的条件下可以生成铜和E,C可在氧气中燃烧生成E和水,而G可由E和黑色固体乙高温反应生成,说明黑色固体乙是碳,E为二氧化碳,G为一氧化碳,C中一定含碳氢元素。
(1)甲乙丙依次是二氧化锰、碳、氧化铜,故填:![]() ,
,![]() ,
,![]() ;
;
(2)反应①是C燃烧能生成二氧化碳和水,说明C中一定含碳氢元素,故C可为甲烷(或酒精),故①的反应方程式为: 或
或 ;
;
反应②是电解水产生氢气和氧气,故反应的方程式为: ,符合“一变多”特征,属于分解反应;
,符合“一变多”特征,属于分解反应;
反应③是氧化铜与一氧化碳的反应产生铜和二氧化碳,故反应的方程式为:![]() 。
。

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】某化学兴趣小组针对教科书中两个实验进行再探究。
(探究一)空气中氧气含量测定的再认识
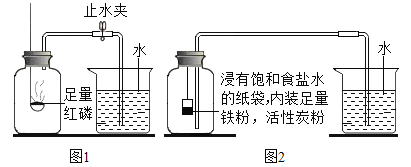
(1)测定装置如图1所示,红磷燃烧消耗氧气,使集气瓶内_____减小,烧杯中的水倒吸进入集气瓶。但该实验误差较大,测得空气中氧气含量明显低于![]() 。
。
(实验改进)根据铁在空气中生锈的原理设计实验如图2所示,装置中饱和食盐水、活性炭能加快铁生锈的速率,测得数据如下表:
实验前 | 实验后 | |
烧杯中水的体积/mL | 烧杯中剩余水的体积/mL | 集气瓶(扣除内容物)和导管的容积/mL |
80.8 | 54.5 | 126.0 |
(2)根据上表信息,空气中氧气的体积分数为_____(只列式,不计算)。
(3)从实验原理角度分析,改进后的实验结果更准确的原因是_____(写一点)。
(探究二)铁在氧气中燃烧后所得固体物质成分的探究
(问题1)铁燃烧时溅落下来的黑色物质中是否含有铁?
(资料)① 自然界中铁的氧化物主要是Fe3O4(黑色)和Fe2O3(红棕色)两种;
② FeO(黑色)极易被氧化为Fe2O3;
③ 铁的氧化物均能与稀盐酸或稀硫酸反应生成铁的化合物溶液。
(实验)将冷却后的黑色物质碾碎,装入试管,加入_____溶液,观察到_____的现象,说明铁燃烧时溅落下来的黑色物质中含有铁。
(问题2)铁燃烧的产物为什么不是Fe2O3?
(资料)① Fe3O4和Fe2O3的分解温度、铁的熔点见表;
Fe3O4 | Fe2O3 | 铁 | |
分解温度/℃ | 1538 | 1400 | — |
熔点/℃ | — | — | 1535 |
② Fe2O3高温时分解成Fe3O4。
(证据推理)根据实验现象及表中信息可知,铁在氧气里燃烧时产生的高温应在_____之间,此时Fe2O3已分解。
(拓展延伸)(1)为了防止集气瓶炸裂,必须采取_____的措施。
(2)某食品密封包装盒的透明盖内放有黑色的FeO粉末,若颜色_____,说明包装盒漏气。
(3)Fe2O3高温时会分解成Fe3O4和一种气体,该反应的化学方程式为_____。
【题目】阅读下面科普短文。
2020年,我国包括北京在内的46个城市,将要推行生活垃圾分类制度。
表1 2016年北京市生活垃圾主要组成的质量分数(%)
厨余 | 纸类 | 塑料 | 玻璃 | 金属 | 木竹 | 砖瓦 | 织物 |
53.22 | 19.60 | 19.59 | 1.25 | 0.15 | 2.83 | 0.60 | 0.72 |
生活垃圾一般可分为四大类:可回收垃圾、厨余垃圾、有害垃圾和其他垃圾。目前垃圾的处理方式主要为填埋、焚烧和堆肥。
垃圾焚烧处置的过程中,很容易产生恶臭气体和酸性气体,如:NO2、SO2等,严重污染自然环境。NO2是大气污染物之一,所带来的环境效应包括:湿地和陆生植物物种之间竞争与组成变化,大气能见度降低,地表水的酸化、富营养化等,还能与空气中的氧气和水化合,形成酸雨主要成分之一的硝酸(HNO3)。
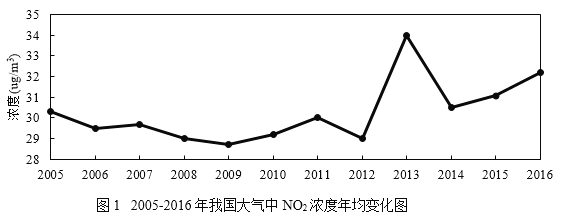
依据文章内容回答下列问题。
(1)由表1可知,2016 年北京市生活垃圾中数量最多的是_____。
(2)矿泉水瓶、旧报纸_______(填“是”或“不是”)可回收垃圾。
(3)酸性气体NO2、SO2中氮、硫元素的化合价为_______。
(4)形成酸雨主要成分之一的硝酸,所发生反应的化学方程式为_______。
(5)请你分析图1,能得到的结论是_______。
【题目】3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 |
| C. | 该物质由碳、氢、氧元素组成 |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |
【题目】在研究酸和碱的化学性质时,某小组想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应。请与他们一起完成实验方案设计、实施和评价。
(1)探究稀H2SO4与NaOH溶液的反应。
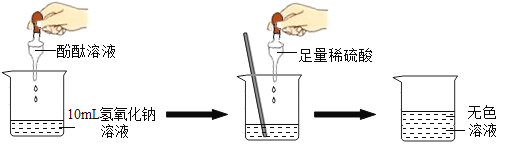
当滴入几滴酚酞溶液后,溶液由无色变为______色。根据上述实验中颜色变化,确定稀H2SO4与NaOH溶液发生了化学反应。反应的化学方程式为______。
(2)探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量。
①根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2、紫色石蕊溶液设计实验方案,请你判断并
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
上述设计的实验方案中,正确的是__________(选填:方案一、方案二)。另外一个实验方案错误的原因是:____________。
②你认为下列药品或方法也能确定稀H2SO4过量的有__________(填字母代号)。
A加入碳酸钠 B加入锌粒 C加入氢氧化镁 D测定溶液pH