题目内容
过氧化钠(Na2O2)是淡黄色固体,常温下,过氧化钠与二氧化碳反应,生成一种盐,同时生成可供呼吸的气体,写出该反应的化学方程式.上述反应生成的正盐的水溶液与CaH2反应,生成白色沉淀,一种气体单质,并测得所得溶液PH>7.其反应的化学方程式为.
【答案】分析:根据可以供给呼吸的气体是氧气进行分析,根据白色沉淀是碳酸钙,气体是氢气,生成物有PH>7的物质进行分析.
解答:解:供给呼吸的气体是氧气,根据质量守恒定律可以知道盐是碳酸钠,过氧化钠和二氧化碳反应生成了碳酸钠和氧气,故答案为:2Na2O2+2CO2=2Na2CO3+O2,
所有的钠盐都溶于水,白色沉淀就只能是碳酸钙,生成的气体是氢气,碳酸钠和氢化钙反应生成碳酸钙沉淀、氢气和氢氧化钠,
故答案为:Na2CO3+CaH2+2H2O=CaCO3↓+2NaOH+2H2↑
点评:在解此类题时,首先根据题中的叙述找出反应原理,然后根据原理找出反应物和生成物,再根据方程式的书写规则进行书写.
解答:解:供给呼吸的气体是氧气,根据质量守恒定律可以知道盐是碳酸钠,过氧化钠和二氧化碳反应生成了碳酸钠和氧气,故答案为:2Na2O2+2CO2=2Na2CO3+O2,
所有的钠盐都溶于水,白色沉淀就只能是碳酸钙,生成的气体是氢气,碳酸钠和氢化钙反应生成碳酸钙沉淀、氢气和氢氧化钠,
故答案为:Na2CO3+CaH2+2H2O=CaCO3↓+2NaOH+2H2↑
点评:在解此类题时,首先根据题中的叙述找出反应原理,然后根据原理找出反应物和生成物,再根据方程式的书写规则进行书写.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案
相关题目
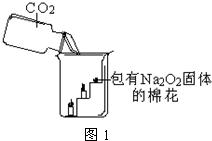


 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
