题目内容
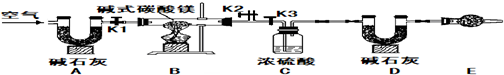
将黑色固体粉末A与白色晶体B混合加热,可产生无色气体C,而黑色固体粉末A在反应前后的质量和化学性质都不变.另一淡黄色固体D在无色气体C中燃烧,生成一种有刺激性气味的气体E,气体E是导致“酸雨”形成的罪魁祸首.
(1)写出物质B的名称:
(2)物质A在上述反应中起
(3)写出D在C中燃烧的文字表达式:
(1)写出物质B的名称:
氯酸钾
氯酸钾
;(2)物质A在上述反应中起
催化(或催化剂)
催化(或催化剂)
作用;(3)写出D在C中燃烧的文字表达式:
硫+氧气
二氧化硫
| 点燃 |
硫+氧气
二氧化硫
.| 点燃 |
分析:在反应前后质量和化学性质没有改变,说明A在反应中起催化作用;淡黄色固体硫能和氧气反应生成有刺激性气味的气体二氧化硫,二氧化硫是导致“酸雨”形成的罪魁祸首,据此展开讨论进行分析即可;A和B都是固体,反应能生成氧气,并且A是催化剂,从而可以判断出A是二氧化锰,B是氯酸钾,C是氧气,D是硫,E是二氧化硫.
解答:解:依据黑色粉末A在反应前后质量和化学性质没有改变,说明A在反应中起催化作用;淡黄色固体D为硫,硫能和氧气反应生成有刺激性气味的气体二氧化硫,二氧化硫是导致“酸雨”形成的罪魁祸首,故E是二氧化硫;A和B都是固体,反应能生成氧气,并且A是催化剂,从而可以判断出A是二氧化锰,B是氯酸钾,C是氧气,D是硫,E是二氧化硫.
(1)由上述分析可知B为氯酸钾
(2)A在反应中起催化作用
(3)D为硫,C为氧气,硫在氧气中燃烧生成二氧化硫,文字表达式为硫+氧气
二氧化硫
故答案为:(1)氯酸钾(2)催化(或催化剂)(3)硫+氧气
二氧化硫
(1)由上述分析可知B为氯酸钾
(2)A在反应中起催化作用
(3)D为硫,C为氧气,硫在氧气中燃烧生成二氧化硫,文字表达式为硫+氧气
| 点燃 |
故答案为:(1)氯酸钾(2)催化(或催化剂)(3)硫+氧气
| 点燃 |
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目