题目内容
18.故事:小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试.于是,他找出一颗生锈铁钉来,放入足量稀盐酸中,然后,美滋滋地去睡觉了…可是,当他醒来之后,发现铁钉不见了,为什么呢?读完了上面的故事,你能用相关的化学方程式解释一下原因吗?Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,Fe+H2SO4=FeSO4+H2↑.分析 把生锈的铁钉放到足量的稀硫酸中,铁锈的主要成分为三氧化二铁,表面的铁锈先与硫酸反应,当铁锈反应完后,铁继续与硫酸反应产生气泡.
解答 解:铁锈的主要成分是Fe2O3,它会与稀硫酸反应,则其化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;当铁锈反应完后,铁继续与硫酸反应,化学方程式为:Fe+H2SO4=FeSO4+H2↑,所以当他醒来之后,发现铁钉不见了.
故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑.
点评 本题难度不大,主要考查酸的化学性质,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
9.在下列实验操作(或措施)与理由的关系中,不正确的是( )
| A. | 用高锰酸钾制氧气时,向高锰酸钾中加入少量MnO2--加快分解速度 | |
| B. | 滴瓶中胶头滴管滴完液体后,立即放回原瓶--防止药液被污染 | |
| C. | 盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞--防止溶液变质 | |
| D. | 实验室贮存白磷时,将其浸没在冷水中--防止发生自燃 |
13.下列可以用“溶解、过滤、蒸发”的操作方法进行分离的是…( )
| A. | 食盐与泥沙 | B. | 铜片与铁片 | C. | 酒精与水 | D. | 食盐与蔗糖 |
3.下列现象描述不正确的是( )
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 铁丝加入硫酸铜溶液有红色固体生成 | |
| C. | 电解水时正、负两极生成气体体积之比为2:1 | |
| D. | 木炭在氧气中燃烧发出白光 |
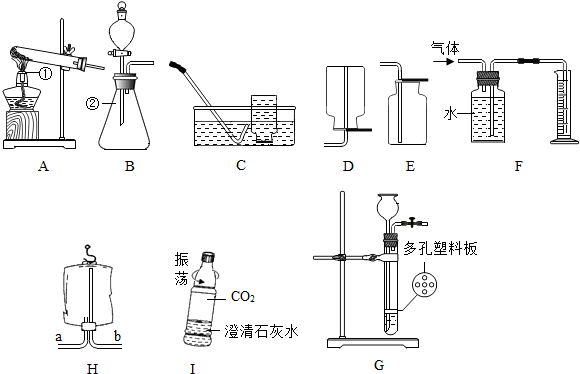
 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.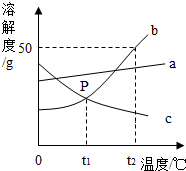 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题: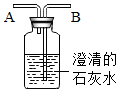 为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验:
为了比较人体呼出的气体和吸入的空气中二氧化碳含量的高低,某化学活动小组的同学设计了如图所示的装置进行实验: