题目内容
A、B两种固体物质的溶解度曲线如图所示.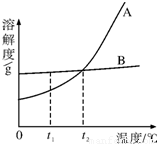
(1)t1℃时,A和B的溶解度大小关系是______;
(2)把t1℃时A的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有______;
(3)t2℃时A的溶解度为25g,在t2℃时,向50g水中加人20g的A物质,充分溶解所得溶液的溶质质量分数为______;
(4)A中混有少量的杂质B,若想得到较为纯净的A,可以采用的方法是______.
【答案】分析:(1)据溶解度曲线可以比较同一温度时物质的溶解度大小;
(2)据饱和溶液转化为不饱和溶液的方法分析回答;
(3)据t2℃时A的溶解度为25g,分析50g水中加人20g的A物质能否完全溶解,并据溶质的质量分数解答;
(4)据AB的溶解度随温度变化分析提纯A的方法.
解答:解:(1)t1℃时,A的溶解度小于B的溶解度;
(2)将饱和溶液变为不饱和溶液还可以采取增加溶剂的方法;
(3)t2℃时A的溶解度为25g,所以50g水中加人20g的A物质最多溶解12.5g,为饱和溶液,溶质的质量分数为: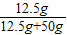 ×100%=20%;
×100%=20%;
(4)A的溶解度随温度的升高而增大,且变化较大,而B的溶解度随温度变化不大,故可通过降温结晶或冷却热的饱和溶液得到较为纯净的A;
故答案为:(1)B>A; (2)增加溶剂; (3)20%;(4)降温结晶或冷却热的饱和溶液.
点评:本题主要考查了固体物质的溶解度曲线的意义及其应用,从而培养学生的理解能力和应用能力.
(2)据饱和溶液转化为不饱和溶液的方法分析回答;
(3)据t2℃时A的溶解度为25g,分析50g水中加人20g的A物质能否完全溶解,并据溶质的质量分数解答;
(4)据AB的溶解度随温度变化分析提纯A的方法.
解答:解:(1)t1℃时,A的溶解度小于B的溶解度;
(2)将饱和溶液变为不饱和溶液还可以采取增加溶剂的方法;
(3)t2℃时A的溶解度为25g,所以50g水中加人20g的A物质最多溶解12.5g,为饱和溶液,溶质的质量分数为:
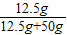 ×100%=20%;
×100%=20%;(4)A的溶解度随温度的升高而增大,且变化较大,而B的溶解度随温度变化不大,故可通过降温结晶或冷却热的饱和溶液得到较为纯净的A;
故答案为:(1)B>A; (2)增加溶剂; (3)20%;(4)降温结晶或冷却热的饱和溶液.
点评:本题主要考查了固体物质的溶解度曲线的意义及其应用,从而培养学生的理解能力和应用能力.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
 22、右图为A、B两种固体物质的溶解度曲线请回答:
22、右图为A、B两种固体物质的溶解度曲线请回答: 如图是A、B两种固体物质的溶解度曲线:
如图是A、B两种固体物质的溶解度曲线: (2013?建宁县质检)A、B两种固体物质的溶解度曲线如图所示:
(2013?建宁县质检)A、B两种固体物质的溶解度曲线如图所示: (2006?平谷区一模)(1)如图为a、b两种固体物质的溶解度曲线.
(2006?平谷区一模)(1)如图为a、b两种固体物质的溶解度曲线. (2012?金山区一模)如图是a、b两种固体物质的溶解度曲线,下列说法中,正确的是 ( )
(2012?金山区一模)如图是a、b两种固体物质的溶解度曲线,下列说法中,正确的是 ( )