题目内容
17.关于反应3Cu+8HNO3(稀)═3Cu(NO3)2+2X↑+4H2O,下列说法不正确的是( )| A. | 铜的化合价由0升至+2 | |
| B. | 可采用制取CO2相同的发生装置制取X | |
| C. | 该反应类型是置换反应 | |
| D. | X的化学式为NO |
分析 A、根据单质种元素的化合价为零、化合物中各元素化合价代数和为零进行分析;
B、制取CO2的发生装置为固液常温型;
C、根据置换反应的概念进行分析;
D、根据质量守恒定律,反应前后原子种类和个数都不变,分别统计出反应前后原子种类及个数,比较分析就可以求出所的物质的化学式.
解答 解:A、铜单质中铜元素化合价为零,在硝酸铜中铜的化合价为+2价,故正确;
B、制取CO2的发生装置为固液常温型,该反应也为固液常温,故正确;
C、该反应的生成物有三种,不属于置换反应,故错误;
D、根据质量守恒定律,反应前后原子种类和个数都不变,由方程式知反应物中含有的原子种类及原子个数为Cu,3;H,8;N,8;O,24;已知生成物中含有的原子种类及原子个数为Cu,3;H,8;N,6;O,22;比较分析可知X中含有N和O元素,其原子个数分别为1,故X的化学式为NO;故正确.
故选C.
点评 此题主要考查学生对质量守恒定律的实际运用,只有掌握了这一知识的内涵,才能自由驾御,正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.钠的下列性质中,属于化学性质的是( )
| A. | 能与水反应 | B. | 有延展性 | C. | 硬度较小 | D. | 密度较小 |
8.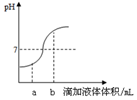 如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
 如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )| A. | 该图象表示的是将稀盐酸滴入氢氧化钙溶液中 | |
| B. | 当滴入溶液的体积为amL时,所得溶液中的溶质只有CaCl2 | |
| C. | 滴入溶液体积为bmL时,再加几滴酚酞试液溶液呈红色 | |
| D. | 恰好完全反应后溶液中存在的粒子只有Ca2+和Cl-离子 |
5.下列对应的实验叙述正确的是( )
| A. |  热水的作用只是提供热量 | |
| B. |  玻璃棒的一端应靠在漏斗右边 | |
| C. |  实验后进入集气瓶中的水约达到刻度4 | |
| D. |  通电实验后试管甲收集到的气体体积比乙少 |
12. 实验室有一瓶无色溶液,标签变得残缺不全(如图所示),同学们设计以下方案探究该溶液的成分
实验室有一瓶无色溶液,标签变得残缺不全(如图所示),同学们设计以下方案探究该溶液的成分
【提出问题】溶液中的溶质是哪种物质?
【作出猜想】
猜想一:溶质为硫酸钠 猜想二:溶质为碳酸钠.
【进行实验】同学们设计了以下三种实验方案进行探究.
【实验评价】同学们讨论后认为方案三设计不合理,理由是硫酸钠也能够与氯化钡能反应生成硫酸钡白色沉淀,他们在方案三的试管中继续进行实验:向试管中滴加足量稀盐酸,观察到沉淀全部溶解,并有气泡冒出(写出实验操作与实验现象).也得出了猜想二正确的结论.
【实验小结】化学实验时应注意保护好标签不被破损,实验后,同学们将这瓶溶液重新贴好标签.放入药品柜.
 实验室有一瓶无色溶液,标签变得残缺不全(如图所示),同学们设计以下方案探究该溶液的成分
实验室有一瓶无色溶液,标签变得残缺不全(如图所示),同学们设计以下方案探究该溶液的成分【提出问题】溶液中的溶质是哪种物质?
【作出猜想】
猜想一:溶质为硫酸钠 猜想二:溶质为碳酸钠.
【进行实验】同学们设计了以下三种实验方案进行探究.
| 实验步骤 | 实验现象与化学方程式 | 实验结论 |
| 方案一:取少量待测溶液于一支试管中,向其中滴加无色酚酞试液(提示:硫酸钠溶液为中性) | 实验现象:溶液变为红色. | 猜想二正确 |
| 方案二:取少量待测液于一支试管中,向其中滴加稀盐酸; | 实验现象:溶液中有气泡产生.化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑. | |
| 方案三:取少量待测溶液于一支试管中,向其中滴加氯化钡溶液 | 实验现象:产生白色沉淀. |
【实验小结】化学实验时应注意保护好标签不被破损,实验后,同学们将这瓶溶液重新贴好标签.放入药品柜.
9.下列变化中与其他之间有着本质区别的是( )
| A. | 煤的干馏 | B. | 百炼成钢 | C. | 石油分馏 | D. | 蜡烛燃烧 |
6.下列排列顺序正确的是( )
| A. | 氯元素的化合价: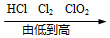 | B. | 溶于水后的水温: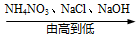 | C. | 地壳中元素含量: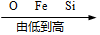 | D. | 铁元素质量分数: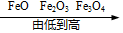 |
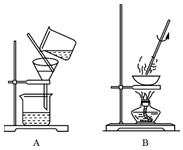 实验室有如图所示装置,回答下列问题:
实验室有如图所示装置,回答下列问题: