题目内容
4. 将质量相等的ab两种金属分别放入质量和溶质质量分数都相同的稀硫酸中,生成氢气质量与反应时间的关系如图所示(反应后无固体残留).下列分析正确的是( )
将质量相等的ab两种金属分别放入质量和溶质质量分数都相同的稀硫酸中,生成氢气质量与反应时间的关系如图所示(反应后无固体残留).下列分析正确的是( )| A. | 两种金属的活动性顺序:a>b | |
| B. | 反应消耗的稀硫酸质量相等 | |
| C. | 反应结束后,图象b所得溶液中的溶质可能有两种 | |
| D. | a、b两种金属可能分别是铁、镁 |
分析 A、根据坐标的斜率b比a大,判断反应的速率;
B、根据生成的氢气的质量分析;
C、根据b生成的氢气少分析;
D、根据等质量的铁和镁与酸反应生成氢气的多少分析.
解答 解:A、根据反应生成氢气的质量与反应时间的关系图可看出,消耗等量的金属b用的时间短,故b比a活泼,反应速率快,故错误;
B、据图象观察a金属生成氢气比b多,反应消耗的稀硫酸质量不相等,故错误;
C、根据图象可知,b产生的氢气少,则消耗硫酸就少,有剩余的硫酸,还有生成b的硫酸盐,溶质可能有两种,故正确;
D、由于等质量的铁和镁与硫酸反应,镁生成的氢气的多,所以a、b两种金属不可能分别是铁、镁,故错误.
故选项为:C.
点评 主要考查了金属和酸溶液的反应的图象从中可以得到什么样的信息,从而培养学生分析问题、解决问题的能力,加强学生对金属活动性顺序的理解

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
12.下列化学用语书写正确的是( )
| A. | 两个氧分子:2O | B. | 铜离子:CU2+ | C. | 氦气:He2 | D. | 氧化铁:Fe2O3 |
19.改善环境、保护环境,应从我做起.下列做法不利于保护环境的是( )
| A. | 将废旧电池深埋,避免重金属污染 | |
| B. | 尽可能少使用一次性纸杯和餐具 | |
| C. | 使用车用乙醇汽油防止“温室效应” | |
| D. | 使用微生物降解塑料和光降解塑料,减少“白色污染” |
9.氢氧化铁[Fe(OH)3]是棕色或红褐色粉末或深棕色絮状沉淀,可用于制造医药、颜料,也可用作砷解毒剂.其可通过6NaOH+Fe2(SO4)3═2Fe(OH)3↓+3Na2SO4反应得来,则该化学方程式中不存在的物质种类是( )
| A. | 无机物 | B. | 氧化物 | C. | 盐 | D. | 碱 |
16.如图所示的实验操作中正确的是( )
| A. |  使用测电笔 | B. |  测量物体的长度 | C. |  测定溶液的pH | D. |  测液体的温度 |
13.区分实验室中的下列各组物质,所用的两种方法都正确的是( )
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 浓盐酸和浓硫酸 | 打开瓶口闻气味 | 分别涂在纸张上观察 |
| B | 黄铜和18K黄金 | 分别加入稀盐酸观察 | 空气中灼烧观察 |
| C | 氯化钠与蔗糖 | 连入电路观察是否导电 | 品尝味道 |
| D | 生石灰和熟石灰 | 加水观察 | 加水后分别加入酚酞试液 |
| A. | A | B. | B | C. | C | D. | D |
14.如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
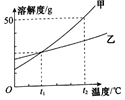

| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯乙 | |
| C. | t2℃时,将甲和乙两种物质的溶液分别降温到t1℃,析出晶体的质量甲一定大于乙 | |
| D. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 |

 水是一种重要的资源,与人类的生活和生产密切相关.
水是一种重要的资源,与人类的生活和生产密切相关.