题目内容
8.某同学模仿物理课上学到的“串联电路”,设计了如下气体制取与性质验证的组合实验.打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降.请看图回答问题: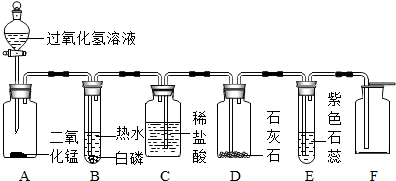
(1)A中发生反应的化学方程式2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,B中白磷能够燃烧的原因是温度达到着火点,有氧气参与.
(2)观察到D中的实验现象是有液体进入D,石灰石表面有气泡产生,E中的实验现象是紫色石蕊试液变红色.
(3)用F装置收集气体的依据是CO2的密度比空气大.
分析 (1)由题意知,反应物为双氧水,生成物为水和氧气,反应条件为用二氧化锰作为催化剂,即可书写其化学方程式;B中白磷能够燃烧的原因,依据燃烧的条件进行解答;
(2)氧气流进入C,则把盐酸压入D和石灰石反应生成二氧化碳,二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;
(3)用F装置是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大.
解答 解:(1)由题意知,反应物为双氧水,生成物为水和氧气,反应条件为用二氧化锰作为催化剂,化学方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;依据燃烧的条件可知B中白磷能够燃烧的原因为与氧气接触;
(2)氧气流进入C,则把盐酸压入D和石灰石反应生成二氧化碳,二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;
(3)用F装置是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大;
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;温度达到着火点,有氧气参与;
(2)有液体进入D,石灰石表面有气泡产生;紫色石蕊试液变红色;
(3)CO2 的密度比空气大.
点评 掌握氧气的反应原理、制取和收集方法;掌握二氧化碳的实验室制法及其物理性质和化学性质;注意燃烧与燃烧的条件.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.生活中废弃的铝质易拉罐、破铁锅、废铜线等可归为一类加以同收,它们属于( )
| A. | 化合物 | B. | 金属或合金 | C. | 氧化物 | D. | 非金属 |
19.某学生俯视量取20mL的水,把水倒掉部分以后,仰视读数是8mL,倒掉的水是( )
| A. | 大于12 mL | B. | 等于12 mL | C. | 小于12 mL | D. | 以上都不对 |
13.下列生活物品中,用有机合成材料制作的是( )
| A. |  铝合金门窗 | B. |  不锈钢餐具 | C. |  塑料洗衣盆 | D. |  景德镇瓷器 |
20.2014年4月,兰州市局部自来水中苯(C6H6)含量严重超标,引发市民恐慌.苯的沸点为80.1℃,熔点为5.5℃,难溶于水,有剧毒,下列有关苯的说法中正确的是( )
| A. | 苯属于无机物 | |
| B. | 苯是由6个碳原子和6个氢原子构成的 | |
| C. | 常温下可通过滤纸过滤的方法除去水中的苯 | |
| D. | 可通过加热蒸发的方法除去水中的苯 |